Pidcc.com.br2
PIDCC – DIREITO CONTEMPORÂNEO E CONSTITUIÇÃO ISSN ELETRÔNICO 2316 -8080 106
Notas Sobre Patentes De Novas Formas Polimórficas
Notes On Patent Of New Polymorphic Forms
Charlene de Ávila Plaza
"Um pais sai prejudicado se concede privilégios monopolísticos em seu mercado
nacional que não melhorem nem tornem mais baratos os artigos disponíveis, nem
desenvolvam sua capacidade produtiva e que não permitam a seus produtores obter
privilégios equivalentes em outros mercados." Edith Penrose (tradução livre).
Atualmente o patenteamento dos denominados segundo uso médico, formas polimórficas e outros elementos têm sido veementemente debatidos nos setores públicos e privados. O presente texto tem como pano de fundo analisar a legalidade, viabilidade e conveniência da exclusiva temporária para as novas formas polimórficas baseado no Ciclo de Discussões Técnicas em Patentes para a Revisão das Diretrizes de Exame do INPI, considerando a problemática referente à interface entre o direito fundamental a saúde e os direitos privados de propriedade intelectual.
Abstract
Currently named after the patenting of medical, polymorphic forms and other elements
have been strongly debated in public and private spheres. This document has the
background to analyze the legality, feasibility and desirability of temporary exclusive for
polymorphic forms based on Cycle Technical Discussions on Patent Review Guidelines
for Examination of the INPI, taking into consideration the issues relating to the interface
between the fundamental right to health and the private rights of intellectual property.
1. Considerações Gerais
Limitações, Exceções e Flexibilidades.
A Lei anterior nº. 5.772/71 não considerava como matéria patenteável
produtos químicos, farmacêuticos, medicamentos e seus processos de obtenção e modificação.
A concessão de patentes relativas à tecnologia farmacêutica foi vedada
por anos com o objetivo de desenvolver e proteger a indústria nacional. Com a promulgação da Lei nº. 9.279/96 que incorporou as flexibilidades contidas no Acordo dos Direitos de Propriedade Intelectual Relacionados ao Comércio (TRIPS) foram revogadas essas proibições.
Dentre as regras do TRIPS incorporadas pela atual legislação nacional,
destaca-se o artigo 27 §1° onde qualquer invenção, de produto ou de processo poderá ser patenteada em todos os setores tecnológicos, desde que respeitados certos requisitos condicionantes, além de estabelecer rol de invenções que podem ser consideradas pelos países membros, como não abarcáveis pela proteção via patentes em suas respectivas legislações.
1 Advogada, Mestre em Direito Empresarial pela Universidade de Ribeirão Preto – UNAERP-SP.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 107
Assim, como toda regra existem exceções, o TRIPS faculta aos países-
membros excluir do âmbito patentário invenções cuja exploração em seu território seja necessária evitar para proteger a ordem pública ou a moralidade, inclusive para proteger a vida ou a saúde humana, animal e vegetal ou para evitar sérios prejuízos ao meio ambiente desde que esta determinação não seja feita apenas porque a exploração é proibida por sua legislaç
Desta feita, não retrata o enunciado, uma proibição explícita de
comercialização como condição de exclusão de proteção, mas a necessidade de tal proibição quando necessário.
A fim de justificar os limites que condicionam a exclusão apregoada pelo
enunciado, os Estados membros devem demonstrar que é necessário para evitar – por qualquer meio – a exploração comercial da invenção.
Já declaração da possibilidade de exclusão do artigo 27§ 2° "não
acontece simplesmente porque a exploração é proibida por suas leis", mas deixa claro que a avaliação da existência ou não da comercialização de uma invenção particular, poderá ser proibida, se necessário, a fim de proteger a ordem pública ou a moralidade não dependendo de positivação de nenhuma legislação nacional.
Entretanto, as regras de flexibilidades e faculdades previstas no TRIPS
sobre a proteção a todos os setores tecnológicos restam condicionadas a certos requisitos técnicos.
Com efeito, o Acordo estabelece um
standard mínimo para a proteção,
deixando para os países-membros a faculdade para conferir uma proteção maior ou mesmo excluí-la.
Verifica-se na lei nacional, o princípio da universalidade das técnicas
onde "qualquer invenção, de produto ou processo, em todos os setores tecnológicos, será patenteável, desde que seja nova, envolva um passo inventivo e seja passível de aplicabilidade industrial".
Entretanto, o TRIPS ao impor padrões mínimos de proteção à
propriedade intelectual para todos os países membros da OMC desconsiderou suas assimetrias gerando um desequilíbrio entre os países detentores e os países usuários de tecnologia.
Na área farmacêutica, esta situação representa obstáculo adicional ao
acesso da população a medicamentos essenciais para a proteção e promoção do direito à saúde e a vida, principalmente pela proliferação progressiva das
2 Assim a regra é: prevê-se a patenteabilidade em todos os setores tecnológicos. No entanto, o Acordo faculta aos países membros excluir do âmbito patentário as invenções contrárias à ordem pública ou a moralidade, inclusive as invenções nocivas à saúde humana, animal e vegetal; plantas e animais, exceto micro-organismos e processos essencialmente biológicos para a produção de plantas e animais, com exceção dos processos não biológicos e microbiológicos, métodos diagnósticos e terapêuticos ou cirúrgicos para tratamento de seres humanos ou animais. PLAZA, Charlene de Ávila. Notas sobre patentes e certificados de cultivares: conflitos ou complementos de proteção? Revista da ABPI, n. 118, mai/jun de 2012, p. 12.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 108
patentes
evergreening que compromete os setores de medicamentos genéricos dos países em desenvolvimento.
Desta feita, a concessão de patentes amplas e difusas gera custos
socioeconômicos, especialmente porque podem ser utilizadas para bloquear ou retardar as invenções de terceiros ou a introdução no mercado de produtos competitivos a preços mais acessíveis.
Geralmente, esta situação assimétrica se faz presente porque a
inovação de fármacos e/ou medicamentos no setor da saúde é dirigida para o mercado onde os investidores estão concentrados nos altos rendimentos, muitas vezes para resolver problemas de saúde nos países desenvolvidos olvidando o desenvolvimento de uma inovação agressiva para as doenças negligenciadas.
Por outro lado, a "lógica" do regime patentário considera que o
monopólio por um período de 20 anos (segundo TRIPS) é indispensável para que as empresas farmacêuticas inovem. O argumento comumente utilizado é que a investigação exige altos custos e as patentes garantem aos mesmos o monopólio temporário que permitem investigar e desenvolver novos produtos.
Cabe argumentar que cada legislação deve visar e regulamentar o
equilíbrio de interesses público e privado, determinar e sobepesar o meio, o modo e as circunstâncias em se conceder ou não o privilégio patentário de acordo com suas idiossincrasias e interesses públicos nacionais. E muito, além disso, é necessária uma leitura adequada do preceito do artigo 27.1 do TRIPS "um elevado critério do que será atividade inventiva" a fim de expurgar as patentes amplas e difusas.
Correasalienta que não existe prova alguma que respalde a tese de
que as patentes geram desenvolvimento e que todos os países, independentemente de seus níveis de desenvolvimento, devam aplicar basicamente as mesmas normas de proteção.
Pelo contrario, atualmente, existem evidencias de que os países
industrializados aumentaram o nível de proteção de patentes à medida que evoluíram e não no sentido inverso.
Geralmente as razões para exceções na maioria das legislações de
propriedade intelectual para a concessão de patentes se inserem em três categorias gerais, a saber:
(i) A análise custo benefício do direito de patentes; (ii) A maior facilidade do funcionamento da Lei de patentes; e
3 BARBOSA, Pedro Marcos Nunes. As patentes farmacêuticas e os direitos humanos. Cadernos da Escola de Direito e Relações Internacionais, v.2, Curitiba, 2009, p. 13.
4 CORREA, C. M. Propriedade Intelectual e Saúde Publica. 1ª edição, La ley, Buenos Aires, 2006.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 109
(iii) A conciliação das celeumas entre o monopólio da patente e outras
metas ou valores sociais (incluindo os direitos fundamentais), vide como exemplo o
Case Oliver Brustle v. Greenpeace
Já a noção de "flexibilidades" pode ser definida como sendo elementos
da legislação de propriedade intelectual que visam permitir países em desenvolvimento a utilizar normas compatíveis com o TRIPS de forma a perquirir suas políticas publicas, tanto em setores específicos como produtos farmacêuticos ou proteção de biodiversidade ou no estabelecimento de condições institucionais, macroeconômicas para dar suporte ao desenvolvimento econômico.
Sujeitas a duas regras básicas, o uso das flexibilidades devem estar em
consonância com o TRIPS e devem reduzir os custos sociais (ou assim considerados pelos países e desenvolvimento) que os direitos de propriedade intelectual geram no tocante a bens protegidos, mas sem diminuir o impacto positivo de tais direitos na promoção da invenção e criação de um ambiente de negócios competitivo (o equilíbrio de direitos e obrigações mencionado no Art. 7° do TRIPS)
5 O Tribunal de Justiça da Comunidade Européia - TJCE no processo C- 34/10 proibiu a concessão de patentes para qualquer processo que envolva a destruição de um embrião humano, incluindo as técnicas usadas na obtenção de células-tronco para fins médicos e pesquisa científica. "Todo óvulo humano deve, desde a fase da sua fecundação, ser considerado um "embrião humano" quando essa fecundação for suscetível de desencadear o processo de desenvolvimento de um ser humano", diz o Acórdão. A Corte considerou que "o óvulo humano não fecundado", no qual foi implantado o núcleo de uma célula humana amadurecida, e o óvulo humano não fecundado que foi estimulado, para efeitos de divisão e desenvolvimento por via de partenogênese, também devem ser qualificados de "embrião humano." Vide PLAZA, Charlene de Ávila. Recentes precedentes da Comunidade Européia em propriedade intelectual. Revista da ABPI, 116, 2012.
6 CARVALHO, Nuno Pires de
. The TRIPS Regime of Trademarks and Designs. USA: Ed.
Kluwer Law International, 2006, p.28-33. What does the word "flexibilities" mean? How can they
impact on TRIPS implementation? 1.74. The TRIPS Agreement itself refers to "flexibility," but
only in connection with the implementation of TRIPS obligations by least-developed country
WTO Members (LDCs).50 That flexibility, as explained infra in comments to the Preamble, is
limited to the methods (and deadlines) for implementing obligations, and not to the substantive
obligations themselves. After Doha, however, the word "flexibility" has been repeatedly used to
refer to those few elements that to some extent reduce the patent rights conferred and that are
commonly referred to in the context of the implementation of the TRIPS Agreement (namely,
international exhaustion, under Article 6; compulsory licenses, under Article 31; and the
regulatory approval exception, under Article 30). In the last years, however, more sophisticated
tools have been identified, which can be used by developing and least-developed countries in
order to reduce the economic, political and social burden that the implementation of TRIPS
standards generally represents (and yet without eliminating their dynamic dimension of
promoting creation and circulation of intangible assets). 1.75. "Flexibilities," therefore, are
those elements of intellectual property law that aim at permitting developing countries to
use TRIPS-compatible norms in a manner that permits them to pursue their own public
policies, either in specific fields like access to pharmaceutical products or protection of
their biodiversity, or in general, such as establishing macroeconomic, institutional
conditions that support economic development.
7 Consoante CARVALHO, Nuno Pires, op. cit.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 110
Note-se que a Declaração sobre Acordo TRIPS e a Saúde Publica
(Declaração de Doha) fez interpretações expressas sobre as flexibilidades e suas aplicações. Na tabela abaixo, será comentado as considerações gerais, as patentes de invenção e o setor farmacêutico.
Natureza
do Direito
Artigo TRIPS
Proteção
Artigo 1.1. Os Membros colocarão em vigor o O Artigo 1:1 obriga a implementacao do disposto neste Acordo. Os Membros poderão, TRIPS pelos membros outorgando
mas não estarão obrigados a prover, em sua flexibilidade fazê-lo da maneira que
legislação, proteção mais ampla que a exigida escolherem, obedecidos aos requisitos
neste Acordo, desde que tal proteção não específicos do Acordo (4 Declaração de
contrarie as disposições deste Acordo. Os Doha, em seu item 5 a) determina na
Membros determinarão livremente a forma aplicação das regras de interpretação do
apropriada de implementar as disposições direito internacional publico que as Não se aplica
Proteção
deste Acordo no âmbito de seus respectivos disposições do Acordo TRIPS devem ser sistema e pratica jurídicos.
interpretadas a luz do objeto e finalidade e
princípios do mesmo.
Art. 6 Para os propósitos de solução de Importação paralela pode ser uma controvérsias no marco deste Acordo, e sem importante ferramenta para acesso a
prejuízo do disposto nos Artigos 3 e 4, nada medicamentos acessíveis tendo em vista a neste Acordo será utilizado para tratar da diferença de valores nos mercados, de questão da exaustão dos direitos de forma que os países em desenvolvimento
propriedade intelectual.
deveriam aumentar o escopo de tal possibilidade e incorporar previsões
explicitas para efetuar um regime internacional de exaustão na legislação
nacional de patentes. Deve-se notar que, enquanto tal flexibilidade e permitida pelo
TRIPS e pela Declaração de Doha, não traduz automaticamente para o regime
nacional e deverão haver dispositivos nacionais específicos . Doha, em seu item 5 d) ainda dispõe que os efeitos das
disposições de TRIPS relevantes para o
Exaustão
esgotamento dos direitos de propriedade intelectual e deixar os membros para
estabelecer o regime de extinção, sem contestação, sem prejuízo da Nação mais Favorecida e tratamentos nacionais relacionados a questões de saúde.
8BARBOSA, Denis Borges. Serviços de Consultoria – Projeto PNUD/BRA/06/036-BSB-Programa das Nações Unidas para o desenvolvimento, 2010.
9 MUSUNGU, Sisuli e OH, Cecília. The Use of Flexibilities in TRIPS BY Developing Countries. World Health Organization, 2006, p. 19.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 111
Natureza do Direito
Artigo TRIPS
Proteção
Art. 27.1. Sem prejuízo do disposto Exige-se para outorga de patentes: novidade,
nos parágrafos 2 e 3 abaixo, qualquer uso industrial e atividade inventiva. Apesar de
invenção, de produto ou de processo, tais características serem já usuais em vários em todos os setores tecnológicos, sistemas antes do TRIPS, o significado de será patenteável, desde que seja cada um destes e objeto de debate. Como
nova, envolva um passo inventivo e examinadores das patentes tem certa seja passível de aplicação industrial. discricionariedade em sua analise, ha
Sem prejuízo do disposto no flexibilidade aos sistemas nacionais . parágrafo 4 do Artigo 65, no No item 27.2 ha discussão sobre a restrição
parágrafo 8 do Artigo 70 e no na interpretação do mesmo. Já no 27.3, a parágrafo 3 deste Artigo, as patentes interpretação deve ser mais restrita, apesar de
serão disponíveis e os direitos haver debates sobre o tema, estando sujeito a patentarios serão usufruíeis sem futuras negociações . discriminação quanto ao local de
invenção, quanto a seu setor No tocante ao Art. 30, membros poderão tecnológico e quanto ao fato de os estabelecer exceções limitadas às exclusivas,
bens serem importados ou
obedecido o teste tripartite:
produzidos localmente.
desde que não conflitem irrazoavelmente com
Patentes
27.2. Os Membros podem considerar o uso normal da patente e não prejudiquem como não patenteáveis invenções irrazoavelmente os interesses legítimos de
cuja exploração em seu território seja detentores de patentes, considerando ainda os necessária evitar para proteger a interesses de terceiros. Os estados poderão
ordem publica ou a moralidade, autorizar a terceiros a produzir o produto ou o inclusive para proteger a vida ou a processo patenteado sem o saúde humana, animal ou vegetal ou consentimento do detentor da patente – para evitar sérios prejuízos ao meio licença compulsória. Tendo em vista o grande ambiente, desde que esta
debate em relação ao alcance
determinação não seja feita apenas apropriado da proteção da patente (não tendo por que a exploração e proibida por a Convenção de Paris estabelecido o âmbito sua legislação.
da cobertura da mesma), as exceções da
27.3. Os Membros também podem mesma também são objeto de controvérsia. considerar como não patenteáveis:
Os negociadores do TRIPS utilizaram a
(a) métodos diagnósticos,
formula de exceções
terapêuticos e cirúrgicos para o prevista pela Convenção de Berna, com tratamento de seres humanos ou de alterações, sem listar exemplificativa ou animais;
taxativamente. Algumas exceções tidas como
(b) plantas e animais, exceto micro-
aceitáveis ate então são: i) importação de
organismos e processos
produto que já foi posto no
essencialmente biológicos para a mercado pelo detentor da patente com seu produção de plantas ou animais, consentimento ou por pessoa autorizada; atos excetuando-se os processos não privados ou em escala e para fins não biológicos e microbiológicos. Não comerciais; iii) uso de invenção para pesquisa, obstante, os Membros concederão experimentação
proteção a variedades vegetais, seja aprovação regulatória para comercializar um por meio de patentes, seja por meio
produto antes da expiração de uma patente; v)
de um sistema sui generis eficaz, seja manipulação de medicamentos em farmácias por uma combinação de ambos. O magistrais; vi) uso da invenção disposto neste subparágrafo será por terceiros que iniciaram ou tomaram atos revisto quatro anos após a entrada de boa fe antes do pedido da patente (ou sua em vigor do Acordo Constitutivo da publicação)
10 Nacoes Unidas. Solução de controversias. TRIPS. 2003, p. 24. Op. Cit.
11 Nações Unidas. Solução de controvérsias. TRIPS. 2003, p. 25 e 26 op. cit. Por exemplo, quanto a "métodos terapêuticos" para o tratamento de humanos, um membro pode argumentar que pode-ser excluir medicamentos da proteção de patentes. O Artigo 27:3(b) não permite esta exclusão para certos produtos e processos "microbiológicos". e Fonte WTO (1994) apud http://equinetafrica.org/bibl/docs/Diss80TRIPSupdate2010.pdf, p. 5.
12CORREA, Carlos. op. cit, p. 302-311. Comenta algumas destas excecoes aceitas: "Experimental use: In the United States, research without the authorization of the patent owner is narrowly admitted for scientific purposes only. (…) In European and other countries, experimentation on an invention (as opposed to with an invention) is allowed even for commercial purposes. (…) With the exception of a few countries, most developing countries have aparently not explicitly used the room left by the TRIPS Agreement to provide for an
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 112
O texto do Artigo 30 deixa um espaço
Art. 30 Os Membros poderão considerável para interpretações, mesmo após conceder exceções limitadas aos o caso Canadá – Farmacêutica Patent A direitos exclusivos conferidos pela licença compulsória (autorização a terceiros patente, desde que elas não conflitem para utilizar patentes sem o consentimento do de forma não razoável com sua detentor da patente) e prevista no art. 31 do exploração normal e não prejudiquem TRIPS. E também autorizada no item 5 b) da de forma não razoável os interesses Declaração Ministerial de Doha: "Cada legítimos de seu titular, levando em membro tem o direito de conceder licenças conta os interesses legítimos de obrigatórias e a liberdade de determinar os terceiros.
motivos pelos quais essas
licenças são concedidas". Os membros estão
Art. 31 Quando a legislação de um também autorizados sob tal artigo a tomar Membro permite outro uso do objeto medidas de forma a prevenir o uso de da patente sem a autorização de seu patentes para praticas anticompetitivas (ou titular, inclusive o uso pelo Governo seja, e ferramenta essencial para equilibrar ou por terceiros autorizados pelo interesses de detentores de patentes e governo, as seguintes disposições públicos). Noutras palavras, a patente não e serão respeitadas: (a) a autorização uma licença para abusar do mercado. desse uso será considerada com Também cobre o uso de patentes por base no seu mérito individual; (b) governos para fins não comerciais, sem limitar esse uso só poderá ser permitido se o âmbito ou estabelecer procedimento dentro o usuário proposto tiver previamente do qual as licenças compulsórias podem ser buscado obter autorização do titular, concedidas (determinando
em termos e condições comerciais emergência nacional ou circunstancia de razoáveis, e que esses esforços não extrema urgência existe, uso não comercial tenham sido bem sucedidos num publico).
doutrina que estabelece
prazo razoável. Essa condição pode condições para a outorga de tais licenças, ser dispensada por um Membro em
incluindo a necessidade de uma analise de
caso de emergência nacional ou mérito individual, exigência de tentativa de outras circunstancias de extrema obter do proprietário da patente em condições urgência ou em casos de uso publico razoáveis por um tempo razoável sem êxito, o nao-comercial. No caso de uso escopo e prazo da licença devem ser limitados publico nao-comercial, quando o ao fim a que se propõe, concluindo-se quando Governo ou o contratante sabe ou as razoes
para tanto terminarem,
tem base demonstrável para saber, primordialmente com clausulas de não cessão, sem proceder a uma busca, que uma para fins predominantes de suprimento do patente vigente e ou será usada pelo Mercado domestico,
experimentation exception, including for commercial purposes. Bolar exception: The so-called 'Bolar' or 'early working' exception deals with the use of an invention relating to a pharmaceutical product to conduct tests and obtain the approval from the health authority, before the expiry of a patent, for commercialization of a generic version, just after such expiry. The purpose of this exception was to help generic drug producers to place their products on the mar ket as soon as a patent expired, and thereby allow consumers to obtain medicines at lower prices immediately thereafter. In exchange, the patent term of the original drug could be extended up to five years. (…) 'Bolar' like exceptions which have been established in numerous countries allow consumers to get access to medicines at a lower price as soon as the patent expires and to support the development of a generic pharmaceutical industry.
13 Nacoes Unidas. Solução de controvérsias. TRIPS. 2003, p. 26.
14 Fonte WTO (1994) apud http://equinetafrica.org/bibl/docs/Diss80TRIPSupdate2010.pdf, p. 5 Note-se, que por vezes a mera ameaça da licença compulsória faz com que o detentor da patente reavalie seu acesso ou estratégia de preço. Nações Unidas. Solução de controvérsias. TRIPS. 2003, p. 27-28. op. cit.
15 "Finally, there are no formalities or prescribed criteria for the determination of what constitutes a national emergency or other circumstances of extreme urgency. A formal declaration by the Member is not required. The determination can be made upon granting the compulsory licence or authorizing government use, or in any other manner." Correa, Carlos M. Trade Related Aspects of Intellectual Property Rights, p.311-345
16 "The 'non-commercial' nature of the use does not prevent the government from appointing a commercial contractor or agent to exploit the relevant patents on behalf of the government, as is common and extended practice in the United States.24 It is also important to note that in accordance with Article 44.2 of the TRIPS Agreement, national laws can limit the remedies available against government use to payments of remuneration in accordance with subparagraph (h) of Article 31; that is, no injunctions may be admitted" Correa, Carlos M. Ibidem.
17 Todas essas condições encontram-se mais comentadas em CORREA, Carlos, op. Cit. 311-345. Especificamente sobre a limitacao de mercado domestico: "The vague wording used does
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 113
ou para o Governo, o titular será remuneração pela licença, sendo outorgado prontamente informado;
ao detentor da patente à possibilidade de
(c) o alcance e a duração desse uso revisão judicial e/ou administrativa da decisão. será restrito ao objetivo para o qual Prevê-se que as leis e praticas que foi autorizado e, no caso de acompanham o licenciamento compulsório tecnologia de semicondutores, será será objeto de controvérsias na OMC na área apenas para uso publico
comercial ou para remediar um procedimento determinado
sendo anticompetitivo ou desleal após um processo administrativo ou judicial; (d) esse uso será nao-exclusivo; (e) esse uso não será transferível, exceto conjuntamente com a empresa ou parte da empresa que dele usufruir; (f) esse uso será autorizado predominantemente para suprir o mercado interno do Membro
not provide specific guidance as to when the domestic market is to be deemed 'predominantly' supplied, National laws may adopt different standards in this respect, based on sales value at volume (eg exports should not exceed an annual average of 50 per cent of net income generated by the product under licence).Developing countries argued in their submission of 12 June 2001 to the Council for TRIPS that 'nothing in the TRIPS Agreement prevents Members from granting compulsory licenses for foreign suppliers to provide medicines in the domestic market . In this respect, the reading of Article 31 (f) should confirm that nothing in the TRIPS Agreement will prevent Members to grant compulsory licenses to supply foreign markets'.25 However, other Members regarded Article 31 (f) as a barrier to such supply, The limitation contained in Article 31 (f) was a central factor in the adoption of paragraph 6 of the Doha Declaration, as examined below.The rationale for this paragraph 6 was as follows. Only a few developing countries have some manufacturing capacity in pharmaceuticals; hence after the TRIPS Agreement became fully operative (on 1 January 2005), many countries could face difficulties in acquiring medicines at affordable prices. Before that date some countries, such as India, produced generic versions of medicines at a fraction of the price of the patented products and could export them to other countries. As a result, a Member country where the price of the patented product was high had the option of issuing a compulsory licence to import it from such countries. The problem was that as these countries became bound to comply fully with the TRIPS Agreement after 2005, they were no longer able to produce and export cheap generic versions of patented medicines. Consequently, countries with insufficient manufacturing capacity could not ensure access to medicines even if they granted a compulsory licence, since they would not be able to find a source for their importation."
18 Ibidem consoante Remuneration Guidelines for Non-voluntary Use o/a Patent on Medical Technologies (James Love, WHO/TCM/2005.1 Geneva, 2005.) "the following are some of the methods of calculation that may be reasonably applied to determine an adequate level of remuneration: a) The 1998 Japan Patent Office Guidelines (applicable to government-owned patents) allow for normal royalties of 2 to 4% of the price of the generic product, and can be increased or decreased by as much as 2%, for a range of 0 to 6%. b) The 2001 UNDP Human Development Report proposed a base royalty rate of 4% of the price of the generic product. This can be increased or decreased by 2%, depending upon such factors as the degree to which a medicine is particularly innovative or the role of governments in paying for R&D. c) The 2005 Canadian Government royalty guidelines for compulsory licensing of patents for export to countries that lack the capacity to manufacture medicines in accordance with the WTO Decision of August 30, 2003. These guidelines establish a sliding scale of 0.02 to 4% of the price of the generic product, based upon the country rank in the UN Human Development Indicator. For most developing countries, the royalty rate is less than 3%. For most countries in Africa, the rate is less than 1 %. d) The Tiered Royalty Method (TRM) method is different from the 200l/UNDp, 1998/]PO or 2005/Canadian methods in that the royalty rate is not based upon the price of the generic product. Instead, the royalty is based upon the price of the patented product in the high-income country. The base royalty is 4% of the high-income country price, which is then adjusted to account for relative income per capita or, for countries facing a particularly high burden of disease, relative income per person with the disease."
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 114
que autorizou; (g) sem prejuízo da proteção adequada dos legítimos interesses das pessoas autorizadas, a autorização desse uso poderá ser terminada se e quando as circunstancias que o propiciaram deixarem de existir e se for improvável que venham a existir novamente. A autoridade competente terá o poder de rever, mediante pedido
fundamentado, se essas
circunstancias persistem; (h) o titular será
adequadamente remunerado
nas circunstancias de cada uso, levando-se em conta
econômico da autorização; (i) a validade legal de qualquer decisão relativa à autorização desse uso estará sujeita a recurso judicial ou outro recurso independente junto a uma autoridade claramente superior naquele Membro; (j) qualquer decisão sobre a remuneração concedida com relação a esse uso estará sujeita a recurso judicial ou outro recurso independente junto a uma autoridade claramente superior naquele Membro; (k) os Membros não estão obrigados a aplicar as condições estabelecidas nos subparágrafos (b) e (f) quando esse uso for permitido para remediar um procedimento determinado
sendo anti-competitivo ou desleal após um processo administrativo ou judicial. A necessidade de corrigir praticas anti-competitivas ou desleais pode ser levada em conta na determinação da remuneração em tais casos. As
competentes terão
recusar a terminação da autorização se e quando as condições que a propiciam forem tendentes a ocorrer novamente; (l) quando esse uso e autorizado para permitir a exploração de uma patente ("a segunda patente") que não pode ser explorada sem violar outra patente ("a primeira patente"), as seguintes condições adicionais serão aplicadas: (i) a invenção identificada na segunda patente envolvera um avanço técnico importante de
significado econômico em relação à invenção identificada na primeira patente; (ii) o titular da primeira patente estará habilitado a receber uma licença cruzada, em termos razoáveis, para usar a invenção identificada na segunda patente; E (iii) o uso autorizado com relação a primeira patente
transferível, exceto com a transferência da segunda patente.
31 bis. 1. The obligations of an Incorporado em 6/12/2005, após a decisão
exporting Member under Article
OMC de 30/08/2003. Considera o fato de que
31 (f) shall not apply with respect
as patentes são outorgadas em território
to the grant by it of a compulsory nacional e nem sempre a
licence to the extent necessary for the proteção será a mesma no pais importador e o purposes of production of a
exportador. O artigo será aplicável:
pharmaceutical product(s) and its a) no pais de importação, se: i) não houver export to an e1igible importing patente no mesmo ou tiver expirado ou
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 115
Member(s) in accordance with the caducado;
terms set out in paragraph 2 of the ii) para produtos ou processos patenteados no Annex to this Agreement.
caso de países menos desenvolvidos ou em
2. Where a compulsory licence is
caso de emergência nacional ou extrema
granted by an exporting Member
urgência (devendo se provar a falta de
under the system set out in this
capacidade produtiva ou sua insuficiência) e,
Article and the Annex to this em todos os casos, houver notificação Agreement, adequate remuneration declaratória ao Conselho do TRIPS para dar
pursuant to Article
transparência, seja de forma qualificada
31 (h) shall be paid in that Member (limitando o uso) ou não. Ha outra taking into account the
possibilidade de notificação relativa a
economic value to the importing
necessidade de produtos .
Member of the use that has been
Existe discussão sobre a utilização de tal
authorized in the exporting Member. flexibilidade para desenvolvimento da Where a compulsory licence is indústria nacional . granted for the same
b) no pais exportador: i)
products in the e1igible importing necessidade salutar em pais estrangeiro após Member, the obligation of that a solicitação de licença voluntaria Member under Article 31 (h) shall not nos limites da necessidade do pais importador apply in respect of those products for com notificação expressa ao Conselho do which remuneration in accordance TRIPS pelo produtor e pelo pais exportador; ii) with the first sentence of this havendo medidas para evitar a reexportação paragraph is paid in the exporting do produto. Member.
Deve haver expressa identificação de que o
3. With a view to harnessing produto e fruto de licenciamento economies of scale for the purposes compulsório
of enhancing purchasing power for, coloração, formato) diferenciado salvo se for and facilitating the local production of, impossível ou tiver um impacto
20 29 Ibidem: "First, the Decision may apply either when a patent covers a product or a manufacturing process. Second, it applies to products 'of the pharmaceutical sector' in general, without any limitation as to the types of products (eg synthesized chemical products or biologicals), their characterization as 'essential medicines', or the kind of diseases they are intended to treat. The Decision clarifies that this concept includes 'active ingredients necessary for its manufacture'. The Decision may be applied in relation to a patent covering a pharmaceutical formulation or the process for its manufacture. The Decision also clarifies that 'diagnostic kits needed for its use would be included'. This wording may be interpreted as including reagents, diagnosis and monitoring kits. Microbiocides can also be considered as covered products. Vaccines are not specifically mentioned in the Decision. (…) Third, reference is made in the examined definition to paragraph 1 of the Doha Declaration, which recognizes' the gravity of the public health problems afflicting many developing and least developed countries, especially those resulting from HIV/AIDS, tuberculosis, malaria and other epidemics' (emphasis added). As the negotiation of the Decision made clear, it applies to pharmaceutical products for any disease. (…) It is unclear whether a patent covering a therapeutic use (generally called 'second indication') is covered by the Decision. The protected invention in this case is a method of treatment and not a product as such. However, such patents can be effectively used to restrict access to the products for important therapeutic purposes. In the absence of an exception, and in view of the intended objectives of the Decision, it seems reasonable to interpret that the Decision can be applied in these cases too."
21Ibidem: "The would-be importing country is bound to notify: (i) the names of the needed product(s): the generic names of the required pharmaceuticals are to be mentioned. (ii) the 'expected quantities': the notified quantities may not exactly correspond to the quantity of product finally requested or purchased. However, importing countries should carefully assess the quantities needed since, as mentioned below, the compulsory licence can be granted in the exporting country for a specified amount only."
22 Ibidem: "This wording suggests that industrial and commercial policy objectives should not be pursued by Member countries under the system established by the Decision, but such objectives are not excluded altogether there from. Thus, eligible importing Members may grant compulsory licences to foster the development of capacity in their pharmaceutical industry as a sustainable way to address their public health problems,31 for instance by importing active ingredients under the Decision for the local formulation of medicines. Further, it seems clear that prospective suppliers of pharmaceutical products under the Decision include private companies, notably from countries where a strong generic industry has developed. Such companies would not make the investments needed nor bear the opportunity costs of supplying products under the Decision, if they are not able to obtain some commercial benefit."
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 116
pharmaceutical products: where a significante no preço. developing or least-
developed Tal flexibilidade também devera sempre ser
country WTO Member is a party to a limitada a necessidade nacional, ser regional trade agreement within the economicamente
meaning of Article XXIV of the GATT possibilidade de alternativas (como genéricos) 1994 and the Decision of 28 disponíveis. November 1979 on
Note-se que o item 5 c) de Doha sobre o tema,
Differential and More Favourable menciona: Treatment Reciprocity and Fuller
"Cada membro tem o direito de determinar o
Participation of Developing Countries que constitui uma emergência nacional ou (L14903), at least half
outras circunstancias de extrema urgência,
of the current membership of which is entendendo-se que crises de saúde publica, made up of countries presently on the incluindo as relativas ao HIV / United Nations list of least-developed "tuberculose, sida e outras epidemias, podem countries,
representar emergência nacional ou outras
the obligation of that Member under circunstancias de extrema urgência." Article 31 (f) shall not apply to the
extent necessary to enable a
pharmaceutical product produced or
imported under a compulsory licence in that Member to be exported to the markets of those other developing or least-developed country parties to the regional trade agreement that share the health problem in question. It is understood that this will not prejudice the territorial nature of the patent rights in question. 4. Members shall not challenge any measures taken in conformity with the provisions of this Article and the Annex to this Agreement under subparagraphs 1 (b) and 1 (c) of Article XXIII of GATT 1994. 5. This Article and the Annex to this Agreement are without prejudice to the rights, obligations and flexibilities that
Members have under the
provisions of this Agreement other than paragraphs (f) and (h) of Article 31, including those reaffirmed by the Declaration on the TRIPS Agreement and Public Health (WT/MIN(0l)/DEC/2), and to their interpretation. They are also without prejudice to the extent to which pharmaceutica1 products produced under a compulsory license can be
23 Ibidem: "There are no parameters in the Decision to determine what a 'significant impact on price' means. Since the Decision's aim is to address public health needs of Member countries-in the framework of the overall objective of the Doha Declaration to ensure access to drugs to all (paragraph 4)-the significance of the increase in price is to be assessed from the perspective of the purchaser. Any increase in price may be 'significant' for the purchaser and limit its capacity to address public health needs, particularly in the case of expensive products or purchases in big volumes. The Decision does not specify either who is going to assess whether the impact is significant or not. It is the supplier who is expected to make this judgement. Though the burden to distinguish the products is on him, the assessment of its impact on price should take the purchasers' interests into account.The statement indicates that 'it is the understanding of Members that in general special packaging and/or special colouring or shaping should not have a significant impact on the price of pharmaceuticals'. This ambiguous statement may be read as a recognition that special packaging, colouring, or shaping does not generally have a significant impact, or as a normative statement emphasizing the idea that the use of such distinction should not have such negative impact. This second reading corresponds to the literal wording of the text. Though it may be seen as redundant, it does clarify that colouring and shaping are alternative and not cumulative, and expresses the Member's concern that the distinction of products must not significantly increase prices. It is important to note that obtaining a compulsory licence may not be sufficient for a company to be able to export a pharmaceutical product under the system, as national health regulations generally require prior approval for the production of medicines for export."
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 117
exported under the provisions of Article 31 (f).28
Fonte: BBARBOSA, Denis Borges. Serviços de Consultoria – Projeto PNUD/BRA/06/036-BSB-Programa das Nações Unidas para o desenvolvimento, 2010.
Barbosa ao discorrer sobre as flexibilidades do TRIPS salienta que o
Brasil falhou em utilizar-se todas as flexibilidades disponíveis:
Brazil, particularly, did not take full advantage of any of the flexibilities when enacting its TRIPs-compliant laws. Even though this relinquishing of flexibilities can not be considered harmonization (as many developed countries retain more access to allowed flexibilities than does Brazil), the pursuance of additional minimum levels through new international agreements may impose dearly on member states abilities to tend to their peculiar needs
2. Sistema Jurídico da Propriedade Intelectual
Note-se, que a nossa legislação de propriedade intelectual é taxativa ao
elencar em seus enunciados matéria que não são considerados inventos (artigo 10); matéria não patenteável (artigo 18), os requisitos objetivos de concessão de patente de invenção (artigo 8° e 24) e seus objetos de proteção, (artigo 42, I e II e art. 183 e seg.). É o que discutiremos a seguir:
A atual lei de propriedade intelectual estabelece claramente requisitos
objetivos condicionantes em face à força vinculante do texto constitucional, as criações, consideradas como tal, se contiverem em seu bojo - novidade, atividade inventiva e aplicabilidade industrial.
A novidade é um dos elementos do balanceamento de interesses
constitucionais para se auferir os benefícios da concessão patentária, "deve ser apurada sob aspecto global daquela solução tecnológica e não sob a ótica dos elementos que a compõem, que poderão, isoladamente, estar abrangidos pelo estado da técnica", (Tribunal Regional Federal da 2ª Turma especializada. Des. André Fontes. AC 204.51.01.513998, DJ 02.07.2008).
Na verdade, o direito de proteção à exclusiva não deve extrapolar a sua
finalidade constitucional para não prejudicar os direitos com ele aparentemente conflitantes – "deve observar no processo hermenêutico a proibição do excesso, de maneira que não ocorra restrição excessiva de qualquer direito
24 BARBOSA, Denis Borges, Research Handbook On The Protection Of Intellectual Property Under WTO Rules, Intellectual Property in the WTO Volume I, Edited by Carlos M. Correa, Director, Center for Interdisciplinary Studies of Industrial Property and Economics, University of Buenos Aires, Argentina.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 118
fundamental, e que haja adequação entre o fim objetivado e o meio empregado".
A aplicabilidade industrial tem como função precípua a repetibilidade em
escala industrial. A invenção deve ser apta a produzir, com os mesmos meios, resultados constantemente iguais, suscetíveis de repetição a fim de estabelecer uma relação de causa e efeito entre os meios utilizados e o resultado obtido e realizados na invenção.
A atividade inventiva é um requisito de equilíbrio de interesses vindo a
reforçar que a invenção não foi antecipada de forma integral por um único documento no estado de técnica, justificando, portanto, a criação de um monopólio resolúvel e temporário.
Deste modo, o que define uma criação como suscetível de proteção
através dos mecanismos de patentes é a sua classificação como invento. É primordial uma contribuição mínima para os estado da técnica, que não seja representativo de criações obvias.
Por tratar-se de uma operação criativa como exercício do intelecto, a
atividade criativa deverá transcender a normalidade das atividades desenvolvidas por um técnico no assunto examinado. Toda invenção se baseia no uso de conhecimentos pré-existentes no estado da técnica.
Diz-se que uma invenção é dotada de atividade inventiva quando ela usa
conhecimentos existentes de uma maneira nunca antes pensada ou sugerida. Para alguns autores o uso de tais conhecimentos anteriores para a solução de um problema técnico de uma forma inesperada deriva mais da intuição do que do raciocínio formal.
Pontes de Miranda ao analisar a convergência dos conceitos de
invenção e atividade inventiva afirma que:
O que importa é que a atividade inventiva ultrapasse o que o técnico da especialidade podia, tal como estava à técnica no momento, achar. O que todos os técnicos da especialidade, no momento, podiam achar não é invenção; não inventa o que diz ter inventado o que qualquer técnico da
25 LEONARDOS, Luiz; OSWALD, Maria Cecília. Direito de patentes: uma resposta de filtragem constitucional. Revista da ABPI, 2007, p. 10.
26MENDONÇA, José Xavier Carvalho de. Tratado de direito comercial brasileiro apud BARBOSA, Denis Barbosa. O Código de propriedade intelectual conforme os tribunais, 2011, p. 131, no prelo.
27 BARBOSA, Denis Borges. Tratado de propriedade intelectual. Seção 5, § 4 – a metodologia para determinar a atividade inventiva. Rio e Janeiro: Lumen Juris, 2010.
28 Inventive level, or
non-obviousness, requires a certain difference from the prior art. How big
the difference should be is a matter of long debate. Elsewhere I have said (and perhaps
demonstrated, or at least tried) that an invention is the connection or combination of two distant
ideas, where a rule of connection did not exist before, said connection being made with an act
of insight or intuition, and not of reasoning. Every invention requires prior ideas (prior art) to be
combined. When the ideas are distant (
i.e., there is no principle of combination), a combination
can not be made with an act of inference, but only with a different faculty of the mind, namely,
insight. Franzosi, Mario -
Novelty and Non-obviousness – The relevant prior Art. Edited
forpublication by Kraig Hill, Toshiko Takenaka and/or Kevin Takeuchi, CASRIP.
29 Miranda, Pontes de. Tratado de Direito Privado. São Paulo: Revista dos Tribunais, v. 4, 1983, p. 274.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 119
especialidade acharia. Porque tal achado estaria dentro da técnica do momento, sem qualquer
quid novum.
A atividade inventiva é um requisito de equilibrio de interesses, "é
preciso que não só haja novidade, mas também que a eficácia e a importância econômica dessa nova técnica seja discernível, de forma que se promova não apenas mínimos aumentos incrementais da tecnologia, e sim algo que seja tão grandioso que justifique a criação de um monopólio instrumental"
Em outras palavras, a atividade inventiva não é somente uma solução
técnica para resolver problemas técnicos. É a solução de um problema por meios não utilizados anteriormente por um técnico no assunto que deve promover um avanço significativo no
state of art, ou pelo menos proporcionalmente ao privilégio em que se requer a exclusiva.
A atividade inventiva é contributo mínimo essencial para a existência de
invenção, "uma possibilidade de perda desnecessária seria a proteção de patente ser conferida para um produto ou processo não inventivo".
Nesse caso a sociedade incorreria em um custo monopolístico de bem-
estar sem obter um produto ou processo novo em troca.
Este ponto, nos alerta para o fato de que, os exames dos requisitos
objetivos referentes à novidade e atividade inventiva de uma criação na lei de patentes devem cumprir a útil função econômica de evitar ganhos monopolísticos não merecidos.
Assim, o abuso potencial de direitos de exclusividade deve ser impedido
pela aplicação rígida dos critérios de exame na lei de patent.
Neste sentido, o tópico seguinte demonstrará alguns dados referentes às
áreas químicas, farmacêuticas e biotecnológicas verificadas junto a ANVISA.
2.1 Da anuência prévia – ANVISA
Com vistas à execução de uma política de saúde pública efetiva, e
considerando que a concessão de patentes amplas e difusas tem impacto negativo no acesso da população à assistência farmacêutica, o governo optou por estabelecer um mecanismo inovador no qual o órgão de saúde passou a integrar o processo de avaliação para concessão de Patentes na área farmacêutica.
30 BARBOSA, Denis Borges et all. O contributo minimo na propriedade intelectual: Atividade Inventiva, Originalidade, distinguibilidade e margem mínima. Rio de Janeiro: Lumen Juris, 2010, p. 10.
31
Aktiebolaget Hassle versus Alphapharm Pty Ltd [2002] HCA 59 (12/12/2002). Disponível em <httpp://www.ipsofactoj.com/international/2003/Part03/int2003(3)-014.htm>.
25/07/2010. "
One possibility whereby an unnecessary dead-weight loss could arise is if patent protection is granted for a non-innovative product or process. In this case society might incur a monopolistic welfare cost without obtaining a new product or process in return. This point alerts us to the fact that the tests of novelty and non-obviousness in the patent law fulfi l the useful economic function of preventing undeserved monopoly profits. This potential misuse of monopoly rights must be prevented by strict application of the screening criteria in the patent law". PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 120
Portanto, os pedidos de patentes de produtos e processos farmacêuticos
passaram a ter sua análise obrigatória pela Agência Nacional de Vigilância Sanitária – ANVISA – desde a Medida Provisória nº 2.006/99, transformada na Lei nº. 10.196, de 2001 que, criou o instituto da prévia anuência, através da inclusão do art. 229-C na Lei nº. 9.279/96.
Ressalte-se que o Acordo TRIPS deixa a critério dos países membros
atribuírem a quaisquer de seus organismos governamentais, isolada ou conjuntamente, o exame para a concessão dos direitos de propriedade industrial, bem como a adoção de normas e procedimentos no âmbito da legislação de propriedade industrial, com vistas à defesa e à promoção da saúde pública. Prevê, ainda, que medidas possam ser adotadas no sentido de promover o interesse público em setores de importância vital para o seu desenvolvimento socioeconômico e tecnológico (Artigo 8.1 do Acordo TRIPS).
No âmbito da legislação nacional, tanto o artigo 5º da Constituição
Federal quanto o artigo 2º da LPI determinam que os direitos de propriedade intelectual são protegidos, considerados o interesse social e o desenvolvimento tecnológico e econômico do País.
Note-se ainda, que quando a patente é concedida, seu titular passa a ter
direitos exclusivos de exploração do objeto protegido (produção, utilização, comercialização, venda ou importação) pelo período de 20 anos. Por isso, há necessidade de análise criteriosa dos requisitos e condições para a concessão da patente, tendo sempre em conta que, especialmente na área farmacêutica, esta proteção implica na criação de um monopólio e na ausência de concorrência com consequente reflexo no preço final do medicamento para a população e para os programas do Ministério da Saúde.
Assim, com o advento do artigo 229C da lei de propriedade intelectual, o
ato que concede ou denega patentes de invenção para produtos e processos farmacêuticos emanam de processo administrativo instaurado junto ao INPI, dependente da prévia e indeclinável anuência da ANVISA. O exame de prévia anuência, além de impedir a concessão de inúmeras patentes amplas e difusas revisou dezenas de impropriedades em pedidos que, na visão do INPI, estariam prontos para o deferimento. Além disso, em vários momentos, o INPI reviu posições suas a respeito de alguns pedidos, após tomar conhecimento dos pareceres da ANVISA. Abaixo, os exemplos de
32O procedimento de prévia anuência para pedidos de patente de produtos e processos
farmacêuticos foi disciplinado recentemente pela Resolução RDC 45/2008. Após um exame
preliminar, o Instituto Nacional da Propriedade Industrial (INPI) encaminha para a ANVISA
todos os pedidos de patentes de produtos e processos farmacêuticos (e não só pedidos de
patente
pipeline), para que a Agência, após exame detalhado de cada pedido, decida por anuir
ou negar anuência a este. A patente só poderá ser concedida após a manifestação positiva da
Agência.
33 O artigo 229C foi introduzido pela Lei 10.196/01 estabelecendo que "a concessão de patentes para produtos e processos farmacêuticos dependerá da prévia anuência da Agência Nacional de Vigilância Sanitária – ANVISA".
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 121
pedidos de patente que não obtiveram prévia anuência da ANVISA, em que o
entendimento do INPI se modificou apenas durante processo judicial proposto
pelo requerente.
Pedidos de patente onde o posicionamento do INPI se alterou durante o
processo judicial:
Resumo do Caso: - Polimorfo de docetaxel reivindicado após rejeição de processo de
obtenção. O docetaxel é usado no tratamento de alguns tipos de câncer.
Da ilegalidade observada: Alteração de matéria – art. 32 – e falta de atividade inventiva do
polimorfo – art.8º c/c 13.
Posicionamento do INPI
Inicial: Aceitou as alterações e aprovou quadro final.
Atual: O pedido foi indeferido pelo INPI, por falta de atividade inventiva do polimorfo –
consequência secundária: o parecer que orientava pela aceitação de modificações em pedidos
foi revogado.
Pedido: PI9507494-5
Resumo do Caso: Reivindicação de compostos intermediários da obtenção de penciclovir e
de famciclovir – antivirais usados no tratamento de herpes.
Da ilegalidade observada: Falta de novidade dos compostos reivindicados – art. 8° c/c 11.
Posicionamento do INPI
Inicial: Considerou que o pedido preenchia os requisitos de patenteabilidade.
Atual: Após demanda judicial, reavaliou o pedido e considerou que o mesmo carecia de
34 Outros exemplos de pedidos de patentes onde ilegalidades foram apontadas no decorrer do
exame de anuência prévia -
O PI9606969-4 refere-se à combinação de uma terapia gênica
com uma técnica convencional, quimioterapia ou
radioterapia, para o tratamento de câncer.
O
PI9509530-6 foi depositado reivindicando composições farmacêuticas tópicas para
administração de macrolídeos, estabilizadas pelo uso de um álcool graxo insaturado, método
de tratamento, uso do álcool graxo e método de estabilização de macrolídeos comum álcool
graxo.
O PI9508927-6 refere-se a um processo de preparação de antiinflamatórios inibidores
de COX-2 e a alguns compostos intermediários.
O PI9508292-1 diz respeito a um processo de
preparação enanciosseletiva de compostos – reivindicações 1 a 25 – e alguns compostos
intermediários.
O PI9608733-1 reivindica um processo de tratamento de isquemia cerebral ou
paralisia, usando um derivado de propargil-aminoindano.
35 O
PI 9508789-3 foi depositado no Brasil em janeiro de 1997 e apresentava cinco
reivindicações para a proteção de um
processo de obtenção do já conhecido princípio ativo
"Tri-hidrato de Taxotere", um importante produto anti-leucêmico e anti-neoplásico, de
fundamental importância no tratamento e recuperação de pacientes acometidos de câncer. No
entanto, reivindicações de processo em pedidos depositados neste período não são
privilegiáveis, de acordo com
o artigo 229-A da Lei nº. 9.279, de 14/05/1996 (LPI).
36 O
PI 9507494-5 requer proteção para intermediários dos princípios ativos Penciclovir e
Famciclovir, que são medicamentos antivirais, usados no tratamento de Herpes. O pedido
descreve e reivindica um processo para a obtenção dos referidos compostos, bem como estes
compostos. Durante o exame no INPI, as reivindicações de processo foram excluídas, tendo
em vista que as mesmas infringiam o artigo 229-A da Lei 9.279/96, que proíbe o
patenteamento de processos farmacêuticos para pedidos depositados no período de
01/01/1995 a 14 de maio de 1997. Com relação aos compostos, embora o INPI tenha
inicialmente apontado a falta de novidade frente a dois documentos do estado da técnica, a
instituição aceita a argumentação que o uso dos compostos no processo em questão resultaria
em maior rendimento e menos etapas de produção e que os compostos não teriam sido
exemplificados nos documentos citados.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 122
Pedido: PI9710536-8
Resumo do Caso: Segundo uso médico de derivados de GABA – para uso no tratamento da
dor, particularmente em dores crônicas.
Da ilegalidade observada: Alteração das reivindicações originais de "método terapêutico" –
art. 10(VIII) – para "uso" – art. 32 - e falta de atividade inventiva do uso pleiteado – art 8º c/c
13.
Posicionamento do INPI:
Inicial: Aceitou as alterações e aprovou quadro final.
Atual: Após demanda judicial, foi exarado parecer considerando que o pedido carece de
atividade inventiva.
Resumo do Caso: Pedido de "patente de seleção", reivindicando proteção para o
valganciclovir – pró droga antiviral usada no tratamento de herpes.
Da ilegalidade observada: Falta de novidade do composto – art. 8º c/c 11.
Posicionamento do INPI:
Inicial: Considerou que o pedido preenchia os requisitos de patenteabilidade.
Atual: Após demanda judicial frente a parecer de perito, exarou parecer considerando que o
pedido não atendia ao requisito de atividade inventiva – tendo em vista que adota
interpretação flexível do requisito novidade.
(Fonte Adaptada: COOPI/GGMED/ANVISA, 2009).
Nas tabelas abaixo, a situação dos processos encaminhados a ANVISA,
os perfis dos impedimentos nas não anuências para as criações mais frequentes e os pedidos não anuídos discriminados por área – ano 2011/12:
Situação dos processos encaminhados á ANVISA – 2012:
37 O
PI 9710536-8 refere-se ao uso de derivados de GABA (ácido gama-aminobutírico) no
tratamento da dor. O pedido foi depositado reivindicando inicialmente um método de tratamento
da dor através da administração destes compostos. Durante o exame no INPI, este quadro foi
alterado algumas vezes, até ser aprovado pelo INPI um quadro reivindicando o uso dos
compostos na preparação de medicamentos para a dor – um novo uso médico.
38 O
PI9503468-4 refere-se ao monoéster de valina do princípio ativo ganciclovir, conhecido por
valganciclovir. O pedido reivindica inicialmente o composto citado e seus sais, bem como suas
composições, seu processo de preparação, seu uso e um método terapêutico caracterizado
pela administração do referido composto ou de seus sais. Durante o exame no INPI, as
reivindicações de processo e uso foram excluídas, por estarem em desacordo com o artigo
229-A da Lei 9.279/96, e as de método terapêutico, por infringirem o artigo 10, inciso VIII, da
mesma lei. Com relação às reivindicações de composto e de composição, o examinador
considerou que as mesmas preenchiam os requisitos de patenteabilidade. A requerente
cumpriu as exigências na íntegra, e o pedido foi encaminhado para a Anvisa, para fins de
prévia anuência.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 123
SITUAÇÃO
QUANTIDADE
Total de pedidos encaminhados
Total de pedidos finalizados
Pedidos não computados nesta análise
Pedidos não anuídos
Pedidos anuídos
FONTE ADAPTADA: COOPI/ANVISA. "SITUAÇÃO DOS PROCESSOS ENCAMINHADOS À ANVISA",
2012. (
*Ainda não concluídos por razões diversas).
Perfil de decisão dos pedidos finalizados:
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 124
FONTE: COOPI/ANVISA, 2012.
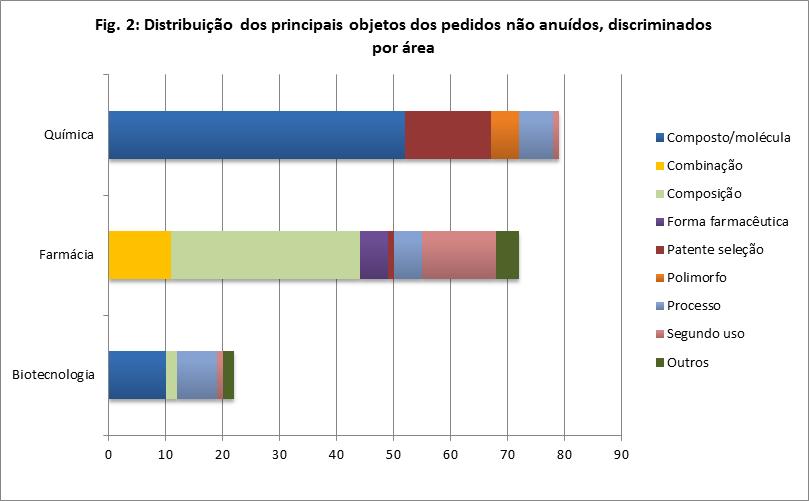
Distribuição dos principais objetos dos pedidos não anuídos,
discriminados por área:
Fonte: ANVISA - Anuência previa – dez. 2011.
Na figura 2, os objetos dos pedidos não anuídos na área farmacêutica
estão na seguinte ordem: composição com maior número de pedidos não anuídos, seguido de criações de segundo uso farmacêutico, combinações, processos, formas farmacêuticas e patentes de seleção em número menor de
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 125
não anuências e, nenhum pedido de formas polimórficas, o que fica
evidenciado que não é usual e nem desejável pedido de proteção para estas
criações no Brasil.
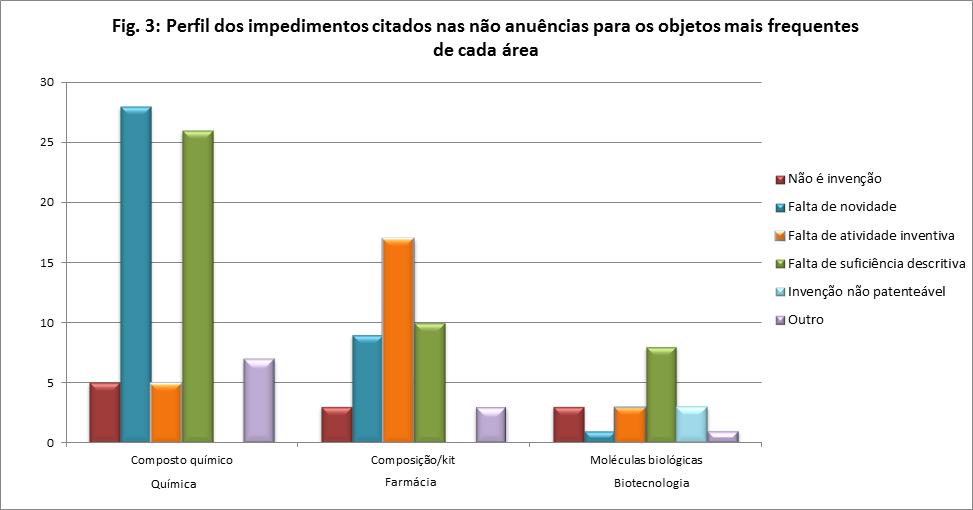
Perfil dos impedimentos citados nas não anuências para os objetos mais
frequentes de cada área:
Fonte: ANVISA - Anuência previa – dez. 2011.
Na figura 3 se percebe que na área farmacêutica (composição/kit) os
impedimentos para as não anuências são em decorrência da constatação da falta de atividade inventiva em comparação com outros requisitos, como não invenção, ausência de novidade, suficiência descritiva e outros. Na área biotecnológica (moléculas) as não anuências ficam por conta da falta de suficiência descritiva e, por fim, na área química (composto químico) a maior incidência de impedimentos é pela ausência de novidade seguida da falta de descrição suficiente para estas criações.
Por todas estas razões, fica evidente que o procedimento previsto no
art.229-C, da LPI, contribui para a proteção e a promoção da saúde pública e vai ao encontro do interesse social, do desenvolvimento tecnológico e econômico do País, na forma dos artigos 5º e 196 da Constituição Federal, de 1988.
Assim, é pertinente salientar que o princípio constitucional sistemático
das patentes requer que, só se defira a exclusiva na presença de uma descrição da nova solução técnica, que capacite qualquer técnico a conhecer o objeto, de forma a aperfeiçoá-lo, se quiser, e a usá-lo livremente ao fim da proteção ou no caso de licença compulsória. O aumento do conhecimento
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 126
tecnológico da sociedade é um dos elementos básicos do equilíbrio constitucional de interesse quanto às patentes.
Além do cumprimento dos requisitos objetivos essenciais para a
concessão de patentes, haverá necessidade da verificação de que não há exclusões incondicionais de patenteabilidade por decisões de política pública abarcados no enunciado do artigo 18 da lei 9.279/96.
3. Das peculiaridades dos artigos 10 e 18 da Lei 9.279/96
O artigo 18 preceitua taxativamente o que não é abarcado por patentes
de invenção, ainda que seja considerado invenção, ainda que sejam novos, tenham atividade inventiva e suficientemente descritos:
Art. 18. Não são patenteáveis: I - o que for contrario a moral, aos bons costumes e a segurança, a ordem e a saúde publicas; II - as substancias, matérias, misturas, elementos ou produtos de qualquer espécie, bem como a modificação de suas propriedades físico-químicas e os respectivos processos de obtenção ou modificação, quando resultantes de transformação do núcleo atômico; e III - o todo ou parte dos seres vivos, exceto os micro-organismos transgênicos que atendam aos três requisitos de patenteabilidade - novidade, atividade inventiva e aplicação industrial - previstos no art. 8o e que não sejam mera descoberta. Parágrafo único. Para os fins desta Lei, micro-organismos transgênicos são organismos, exceto o todo ou parte de plantas ou de animais, que expressem, mediante intervenção humana direta em sua composição genética, uma característica normalmente não alcançável pela espécie em condições naturais.
Aqui se trata de norma proibitiva por questões de políticas públicas e
não norma meramente classificatória, como no caso dos enunciados do artigo 10 da lei 9.279/96.
O artigo 10 abarca os objetos que não são considerados inventos:
I - descobertas, teorias cientificas e métodos matemáticos; II - concepções puramente abstratas; III - esquemas, planos, princípios ou métodos comerciais, contábeis, financeiros, educativos, publicitários, de sorteio e de fiscalização; IV - as obras literárias, arquitetônicas, artísticas e cientificas ou qualquer criação estética; V - programas de computador em si; VI - apresentação de informações; VII - regras de jogo;
39 BARBOSA, Denis Borges. Tratado de propriedade intelectual. 5] § 2.1. Um exemplo: a novidade no caso de cultivares. Rio de Janeiro: Lumen Juris, 2010, p. 312.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 127
VIII - técnicas e métodos operatórios ou cirúrgicos, bem como métodos terapêuticos ou de diagnostico, para aplicação no corpo humano ou animal; e. IX - o todo ou parte de seres vivos naturais e materiais biológicos encontrados na natureza, ou ainda que dela isolados, inclusive o genoma ou germoplasma de qualquer ser vivo natural e os processos biológicos naturais.
Os itens I, II, IV e IX do artigo 10 são hipóteses de criações que não
apresentam utilidade – "tem-se efeito de conhecimento ou de criação expressiva, mas nunca a solução de qualquer problema prático (se o conhecimento leva a uma utilidade, "descoberta" já não e, mas aplicação útil, assim suscetível de inclusão na categoria de invento)".
Os itens, III, V, VI, VII do mesmo artigo, são hipóteses de criações que
são úteis, mas somente práticas – e não técnicas.
Em tais hipóteses será denegada a pretensão de patente enquanto não
importarem na solução de um problema técnico.
De outro lado, o artigo 10 lista duas hipóteses que não se enquadram
em nenhuma das duas hipóteses:
VIII - técnicas e métodos operatórios ou cirúrgicos, bem como métodos terapêuticos ou de diagnostico, para aplicação no corpo humano ou animal; e IX - [o todo ou parte de seres vivos naturais e materiais biológicos encontrados na natureza,] ou ainda que dela isolados [inclusive o genoma ou germoplasma de qualquer ser vivo natural e os processos biológicos naturais].
O primeiro caso e listado no art. 27 de TRIPs como hipótese de rejeição incondicional de patenteabilidade, havendo ou não invento. O acordo Internacional permite que nestes (e nos casos listados no art. 18 da Lei 9.279/96) os estados membros possam denegar patente, em qualquer hipótese, e sem considerar se ha ou não invento, novidade, atividade inventiva, ou aplicação industrial. Seguramente as técnicas e métodos operatórios importam em soluções de problemas não só práticos, mas técnicos. Em muitos casos, tais práticas carecerão de aplicabilidade industrial sob o art. 15 212; mas a exclusão de patenteabilidade não se cinge somente a tais hipóteses. A Convenção Europeia de Patentes, como a lei brasileira, listava tais casos como carecedores de invento. Em sua alteração de 2000, no entanto, tal erro topológico foi corrigido, estando às hipóteses agora listadas entre as exclusões incondicionais.
Diversamente das matérias do enunciado do artigo 18 da lei 9.279/96
que regulamenta as criações insuscetíveis de proteção por patentes de invenção por interesses de política pública, o artigo 10, da referida Lei, abarca
40 BARBOSA, Denis Borges, op. cit., p. 127.
41 BARBOSA, Denis Borges, op. cit., p. 127-128.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 128
as criações que não são sujeitas a privilégios, muito embora, em algumas situações serem consideradas inventos.
Sob a égide do artigo 10, não se apregoa a não patenteabilidade das
criações, e sim, as que não comportam, em tese, o privilégio de proteção até o momento que inexistir uma solução técnica para problemas técnicos porque seu enunciado é uma declaração de fato do que não é, presumivelmente, invento.
Não há nos enunciados do artigo 10, quaisquer referências de natureza
proibitiva a concessão de patentes. São enunciados que condiciona a proteção a certos e restritos pressupostos, quais sejam:
• a existência de um invento, •dotado de novidade, •qualificada a novidade pela atividade inventiva, •suscetível de aplicação industrial, •sendo que se verifica a suficiência
descritiva de seu requerimento, de forma a permitir eficazmente a reprodução do invento na indústria e como insumo de pesquisa.
Verifica-se, portanto, que existem duas situações limítrofes na lei de
propriedade intelectual brasileira:
(i) De natureza declaratória – sujeita a uma condicionante prevista no
enunciado 10, por não reconhecer nestas criações a natureza de invento
enquanto não representarem uma solução técnica para um problema utilitário
técnico – (Aqui poderíamos inserir as criações de formas polimórficas);
(ii) De natureza proibitiva – previstas no artigo 18, por questões de política
pública, ainda que estas criações sejam consideradas invenções, sejam novas,
tenham atividade inventiva e possam ser suficientemente descritas (exceto as
criações que a própria lei condiciona a patenteabilidade seguindo algumas
condicionantes).
4. Considerações Específicas
Das novas formas polimórficas - O problema
Recentemente, tem sido debatido e questionado o patenteamento de
certos objetos, cuja característica central é permitir a manutenção do regime protetivo a certas facetas da tecnologia - o patenteamento do segundo uso médico, os inventos de seleção, os polimorfos, os enantiômetros e pró- drogas.
Conceder ou não patentes para estes tipos de criações engloba não
somente exames técnicos precisos para aferição dos requisitos objetivos como também a observância aos direitos relacionados à saúde e a vida e princípio constitucional sistemático das patentes que assegura o desenvolvimento econômico, social e tecnológico.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 129
Desta forma, o legislador condicionou o direito de se obter exclusiva a
certos critérios objetivos subordinados sempre aos interesses sociais, políticos e tecnológicos de cada país. Desta declaração é importante salientar que muito embora os critérios de patenteabilidade seguirem os mesmos requisitos objetivos em quase todas as legislações nacionais, o entendimento sobre o que seja atividade inventiva não é homogêneo.
Em especial as criações de novas formas polimórficas, o INPI emitiu
para consulta publica uma proposta de diretriz de exame espelhado na abordagem "problema/solução" para a atividade inventiva (problem and solution approach) utilizada pelo Escritório de Europeu de Patentes - EPO. Contrario a posição do INPI (a favor do patenteamento desses objetos), foi proposta legislação que a denega.
42 "A atividade inventiva de uma forma polimórfica será aferida ao se constatar um efeito que solucione um problema do estado da técnica suficientemente diferenciador, como por exemplo: aumento na estabilidade, solubilidade aparente e processabilidade. Uma vez que não há nenhum conhecimento geral que torne possível a previsão das propriedades de um polimorfo, não seria óbvio produzir uma nova forma cristalina na expectativa de resolver um determinado problema técnico. Ainda que se saiba que diferentes formas polimórficas possam apresentar características inesperadas, não há como prever, pelos conhecimentos comuns, quais serão os novos efeitos técnicos obtidos, pois isto somente será conhecido quando as formas polimórficas forem identificadas, caracterizadas e testadas para os efeitos desejados."
44 PL n. 2.511/2007 e seu apenso PL n. 3995/08, que busca proibir a concessão de patente aos
polimorfos e aos segundo uso medico: Acrescenta incisos ao art. 10 da Lei n° 9.279, de 14 de
maio de 1996, que regula direitos e obrigações relativas à propriedade industrial:
O Congresso Nacional decreta:
Art. 1º O art. 10 da Lei nº 9.279, de 14 de maio de 1996,
passa a vigorar com a seguinte redação:
"Art. 10 I – (.), VIII – técnicas e modelos operatórios ou cirúrgicos, bem como métodos
terapêuticos ou de diagnósticos, para aplicação no corpo humano ou animal; XIX – (.) X –
nova forma cristalina de substância compreendida no estado da técnica; e XI – modificação de
produto ou substância terapêutica objeto de patente, para o qual foi constatado utilidade ou uso
diverso àquele explorado pelo titular da patente. (NR)" Art. 2º Esta lei entra em vigor na data de
sua publicação oficial.
Importante observar alguns equívocos no PL n° 3995/08. O PL diz que "O art. 10 da Lei n°
9.279/96 descarta o patenteamento do que não se considera como invenção". Entretanto,
o artigo 10 não descarta o patenteamento, ele simplesmente reza o que não é invenção até o
momento que a criação represente a existência de um invento, dotado de novidade, qualificada
a novidade pela atividade inventiva, suscetível de aplicação industrial, sendo que se verifica a
suficiência descritiva de seu requerimento, de forma a permitir eficazmente a reprodução do
invento na indústria e como insumo de pesquisa. Diz também que "A expressão "métodos
terapêuticos" é ampla. Significa o procedimento – prescrição de uso de um ou mais
medicamentos de dietas, de radiação ionizante, de atividade física ou de fisioterapia,
etc., combinados ou não adotados pelo médico na terapia de uma patologia ou de uma
síndrome. O termo "protocolo" tem sido usado no meio médico com sentido de método
terapêutico em que há a intervenção mais ou menos padronizada de medicamentos e
outras formas de terapias. Desse modo, nem o uso combinado de terapias, nem o uso de
apenas um medicamento pode ser patenteado". "A patente de segundo uso também
impede, ao final do prazo da patente original, que outras empresas farmacêuticas
explorem com medicamentos similares o novo campo descoberto". Equivocam-se os
legisladores mais uma vez: Tal reivindicação não colide necessariamente com a vedação aos
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 130
Veja na tabela abaixo, que a situação não é diferente no Direito
comparado, cujas legislações não trazem menção específica para a proteção destas criações, com exceção da lei indiana que legalmente regulamenta a questão, condicionando-as aos requisitos de patenteabilidade e particularmente ao aumento da eficácia:
Situação dos pedidos de patentes –
formas polimórficas
África do Sul
Sem menção específica na lei ***
Argentina
Sem menção específica na lei ***
Menção específica nas diretrizes de exame,
condicionado aos requisitos de patenteabilidade, como exemplos de depósitos concedidos *.
Comunidade Andina
Sem menção específica na lei
Sem menção específica na lei; com exemplos de patentes concedidas. *
Sem menção específica na lei; com exemplos de patentes concedidas. ****
Sem menção específica na lei; com exemplos de patentes concedidas. ****
Expressamente regulamentada em lei a
questão das formas polimórficas,
condicionando aos requisitos de patenteabilidade e particularmente ao aumento da eficácia. ** Com exemplos de patentes concedidas. *
Sem menção específica na lei; com exemplos de patentes concedidas. ****
Sem menção específica na lei; com exemplos de patentes concedidas. *
Fonte: Raimundo Jorge. Patentes polimórficas e patentes de segundo uso médico, 2009. * Sem acesso ao quadro reivindicatório concedido. ** conforme o item 3(d) do The Patents (Amendment) Act, 2005, Índia. *** andamento dos pedidos não disponível nas bases de dados. **** quadros reivindicatórios analisados quanto à matéria concedida (produto, processo, composição e uso).
métodos de tratamento e diagnósticos, prevista no art. 10, VIII da Lei. 9.279/96, desde que o relatório descritivo suporte uma reivindicação dirigida a um fim dotado de utilidade industrial.
45 O USPTO tem concedido algumas patentes, por exemplo, US 20050131067, com a seguinte reivindicação: 1. A crystalline tolterodine tartrate form 1, characterized by na x-ray powder diffraction spectrum having peaks expressed as 2 theta at about 11,9, 13.6, 14.2, 15.9, 16.9, 18.4, 18.8, 20.4, 22.0, 23.9, 25.4, 26.3, and 29.8 degrees. Os analistas entendem que seja duvidosa a confirmação de patente no judiciário, em face do padrão mais alto de atividade inventiva suscitado pela Suprema Corte em KSR v. Teleflex, em 30 de abril de 2007. Até aos anos 60, o USPTO e as cortes americanas seguiam a doutrina de avaliar a atividade inventiva através da pergunta se o pedido de patente era "obvious to try", prima facie. Se a resposta fosse positiva não havia atividade inventiva. Posteriormente e por muitos anos, passou-se a seguir a doutrina Papesch que dizia que, mesmo que fosse óbvio tentar, se o produto resultante apresentasse propriedades inesperadas haveria atividade inventiva. A aplicação indiscriminada da doutrina Papesch levou a concessão de uma enxurrada de patentes de duvidoso mérito, situação que agora a Suprema Corte dos EUA tenta corrigir com sua decisão no caso KSR x Teleflex.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 131
A abordagem problema/solução desenvolvida pela jurisprudência do
EPO para se verificar a atividade inventiva baseia-se no princípio de que "toda invenção representa uma solução técnica para um problema técnico impedindo, assim, vícios das análises ex post facto, prejudicadas pelo conhecimento posterior do reivindicado na patente. Desta forma, um invento, para ser patenteável, será técnico em seu objeto, em sua aplicação e em seu resultado; só então esse invento será avaliado quanto à novidade, inventividade e a legalidade.
O INPI, por sua vez propõe que:
1.9.2.2 Atividade inventiva
Uma vez aferida à novidade de determinada invenção de um pedido de
patente de invenção, o examinador verificará a existência de atividade
inventiva. A existência de novidade é pré-requisito essencial para a
existência de atividade inventiva. Na aferição da existência de atividade
inventiva deve-se considerar se um técnico no assunto, que conhecesse à
época as citações do estado da técnica consideradas, teria sido motivado
a realizar a combinação ou modificações necessárias para chegar à
invenção em questão. Tal aferição só pode ser baseada em documentos
publicados antes da data de depósito ou da prioridade do pedido.
Algumas situações onde há falta de atividade inventiva podem ser
elencadas, sem, no entanto serem exaustivas. Nesses casos, em princípio,
há falta de atividade inventiva quando não há efeito técnico novo: - mera
escolha ou troca de material cujas propriedades são conhecidas; - mera
mudança de forma e/ou proporção; - mera justaposição de meios
conhecidos; Alguns fatores podem ser considerados como indícios da
existência da atividade inventiva: - dados comparativos em relação ao
estado da técnica que mostram a superioridade da invenção e são
convincentes na demonstração da atividade inventiva; - existência de
problema técnico cuja solução era necessária e desejada há muitos anos e
a invenção é a resposta a esta necessidade; - a solução apresentada pela
invenção é contrária as atividades normais na mesma área técnica e um
técnico no assunto não pensaria em seguir o mesmo caminho; - sucesso
comercial, se vinculado ao caráter técnico da invenção, e não devido à
publicidade.
46 Para precisar o alcance do pedido do privilégio, é necessário declinar o campo técnico no qual o invento se insere; para que a publicação seja eficaz como pressuposto da patente, é preciso assegurar que o problema técnico e sua solução sejam entendidos; as reivindicações descrevem as características técnicas do invento. Barbosa, Denis Borges. Tratado de propriedade intelectual – Patentes – Tomo II, Rio de Janeiro: Lumen Juris, 2010, p. 1111.
47 Or l'nvention pour être brevetable doit avoir um caractere industriel, dans son objet, son application et son resultat. L'enonciation des trios termes est cumulative. Cela étant, l'expression la plus importante est dans doute celle d'application. Car si l'invention est applicable industriellement, elle a generalement um objet et um resultat insdustriel. Pollaud Dullian. La brevetabilité dês inventions, Litec, 1997, p.41 e seg. Chavanne e Burst. Droit de La propriété industrielle, Dalloz, 1990, n. 16 e seg., p. 33-34. (Ora a invenção, para ser patenteável, deve ter um caráter industrial, em seu objeto, sua aplicação e seu resultado. A enunciação dos três termos é cumulativa. Tanto será a expressão mais importante restará sem dúvida desta aplicação. Pois se a invenção é industrialmente aplicável, ela geralmente terá um objeto e um resultado industrial).
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 132
Ao contrário da proposta do INPI, que não possui clareza e tratamento
analíticos desejáveis, a abordagem do EPO desenvolve critérios mais estritos, como por exemplo, seguindo três etapas básicas e sucessivas:
(i) Determining the "closest prior art"; (ii) Establishing the "objective technical problem" to be solved, and (iii) considering whether or not the claimed invention, starting from the closest prior art and the objective technical problem, would have been obvious to the skilled person" (2007, part C, IV-24).
Assim, as diretrizes da EPO abrangem passos básicos, predeterminados
e sucessivos: (i) o estado da técnica mais próximo; (ii) o problema técnico a ser resolvido e, (iii) em se verificando o estado da técnica mais próximo, a suposta invenção não seria óbvia para um técnico no assunto.
Souto Maiornos diz que a abordagem problema/solução é apenas
uma entre as várias análises possíveis para a verificação da atividade inventiva:
O EPO, onde o método se desenvolveu, já explicitou o fato em casos com T_0465/92 em que a abordagem não foi aplicada. Nos EUA o método de aferição é outro, feito a partir dos Grahan factors: (a) aferir o Estado de Arte ao tempo da invenção; (b) traçar diferenças entre o reivindicado e ao Estado de Arte; (c) examinar se um técnico no assunto teria tal diferença por óbvia; além das considerações secundárias, como sucesso comercial ou prévias tentativas fracassadas.
A posição do EPO não é seguida uniformemente por todos os países da
comunidade europeia. Há divergências de interpretação, por exemplo, com os escritórios do Reino Unido e da Holanda A interpretação do UKPOé mais
48 SOUTO MAIOR, Rodrigo de Azevedo. As possibilidades da atividade inventiva no Brasil: uma busca no direito comparado pelos modos de aferição objetiva do critério de patenteabilidade, apresentada ao Programa de Mestrado em Direito Internacional da Faculdade de Direito da Universidade do Estado do Rio de Janeiro, 2009.
49 Para uma análise consistente, a abordagem problema/solução não deve ser o único teste com que se deve aferir a atividade inventiva. Para maior rigor na análise as diretrizes devem ainda fazer uso da metodologia usada no USPTO, a do Teste Sugestão-Motivação com a recente interpretação da Suprema Corte americana no caso KSR x Teleflex, complementado pelo uso dos fatores de Graham,
adaptados a prática brasileira, Vide:
50 A jurisprudência recente da Suprema Corte (KSR v. Teleflex, 550 U.S, 127 S. Ct, 1727 (2007) remodelou os critérios de aferição, fazendo mais rígido o exame da atividade inventiva ao expandir o nível abstrato de criatividade do técnico no assunto. Manteve, todavia, dois pilares importantes, cujas tensões devem ser equalizadas: a necessidade de respeito à cláusula constitucional do contributo mínimo e a procura por meios objetivos de proteção contra as análises ex post facto viciadas.
51 A validade de patentes de formas sólidas é criticada em importantes jurisdições da Europa. Embora o EPO conceda estas patentes as cortes (especialmente a corte holandesa e a Inglesa) nem sempre reconhecem a validade das mesmas. Ver por exemplo o recente caso da Warner Lambert, onde o sal de cálcio da atorvastatina foi considerada válida nos EUA, mas
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 133
restritiva que a do EPO e a interpretação da corte de justiça inglesa ainda mais
restritiva que a do UKPO.
5. POLIMORFISMO – Definição e Características
Polimorfismo e a capacidade de um determinado sólido adotar duas ou
mais conformações cristalinas.
Essa propriedade, intrínseca à substância, pode conduzir a diferentes
propriedades físico-químicas, termodinâmicas, etc. Na indústria farmacêutica, também são classificados como polimorfos – ou, mais especificamente, pseudopolimorfos – as formas sólidas onde moléculas de solvente são incorporadas à rede cristalina, formando solvatos. Como consequência, vários problemas podem ocorrer, tanto na fabricação, quanto no armazenamento, e até mesmo na utilização daquela substância.
No caso dos medicamentos, essas alterações podem ser
particularmente relevantes, pois podem afetar sua biodisponibilidade, tornando-os ineficazes, ou até mesmo tóxicos .
Em outras palavras, polimorfos são diferentes formas cristalinas de uma
mesma substância. Cada forma cristalina é distinta da substância original (forma amorfa), e pode ou não apresentar propriedades distintas, que podem ser viáveis para o uso terapêutico.
Assim, as características intrínsecas do polimorfismo são: (i) a
capacidade de uma mesma substância se apresentar no estado sólido sob mais de uma forma cristalina, isto é, rearranjar seus átomos sob formas não na Inglaterra e Holanda (Países Baixos), ou os casos da claritromicina, onde a patente do polimorfo foi considerada não inventiva inter alia de acordo com a corte holandesa.
52 Recentemente o UKPO fez uma consulta publica quanto à aplicação que vem fazendo do conceito de atividade inventiva e o resultado apoiou uma interpretação rígida para evitar a concessão de patentes triviais, mas sem fechar a porta para a concessão de patentes que viessem realmente trazer contribuições significativas ao estado da arte.
53 LIMA, Denise M. Menezes de; SILVEIRA, Carla Cristina de Freitas. Physis Revista de Saúde Coletiva. Rio de Janeiro, 2011, p. 1520-21.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 134
diferentes; (ii) a decorrência de uma propriedade intrínseca, isto é, inerente à substância; (iii) as diferenças físico-químicas e alteração na biodisponibilidade, entretanto, atendendo à mesma finalidade ou função.
6. Patentes de novas formas polimórficas e suas consequências
Gama Cerqueira preconiza que "os elementos característicos da
invenção devem ser examinados e apreciados de acordo com a função que desempenham e não sob o seu aspecto material (.) este princípio aplica-se a todas as espécies de invenção e é particularmente importante quando se trata de invenções de processo".
Note-se que quando se trata de aferição de patentes para novas formas
polimórficas é necessário verificar se o processo em que se pede a exclusiva não esteja evidenciado em patente original, fato que prolongaria seus efeitos além do previsto em lei, ferindo frontalmente o direito de concorrência e a segurança jurídica.
Dessa forma, existem questões de extrema relevância quando estas
criações adentram o campo da propriedade intelectual principalmente no que tange:
(i) Às próprias ambiguidades dos polimorfos quando na oportunidade do exame técnico para se verificar os requisitos legais e constitucionais a concessão do privilégio; (ii) Aos impedimentos à entrada de medicamentos genéric pela perpetuação da exclusividade de mercado e dos preços do monopólio de medicamentos devido à extensão da proteção patentária além dos parâmetros legais e, (iii) O aumento do número de litígios judiciais pela dificuldade de se limitar o escopo da suposta "invenção", todas inviabilizando as políticas de saúde pública.
54 CERQUEIRA, João da Gama. Tratado de propriedade intelectual, v.II, tomo I, parte II, Rio de Janeiro: Revista Forense, 1952, p. 320.
55 Como se trata de uma nova forma cristalina de um composto químico conhecido, para a caracterização da novidade é essencial verificar se esta forma cristalina já não se encontrava presente no composto existente antes da data do depósito do pedido ou da prioridade reivindicada. Desta forma, para a concessão do privilégio deve ser exigida a caracterização da forma cristalina existente no estado da técnica, sem o que não ficará caracterizada a novidade do presumido novo polimorfo. Todos os parâmetros técnicos exigidos para caracterizar o novo polimorfo devem ser igualmente disponíveis para a forma sólida do produto conhecido ou da patente anterior, se for o caso. Vi
56 O exemplo do medicamento anti-retroviral Ritonavir, que está em domínio público no Brasil, nos mostra na prática os efeitos das patentes de polimorfos. Existem pedidos de patentes de formas polimórficas do princípio ativo do Ritonavir que, se concedidas, impediriam a produção dos respectivos genéricos.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 135
Além disso, os polimorfos por serem considerados como uma
propriedade intrínseca da substância, isto é, uma propriedade inerente à matéria em seu estado sólido, é de crucial importância à verificação de que os processos em que se pede a proteção de uma nova forma polimórfica não sejam inerentes da sua própria natureza, despidos de atividade inventiva.
Por outro lado, o processo de obtenção de um polimorfo poderá ser
abarcado pela exclusiva a partir do momento que resolver um problema técnico diverso do anteriormente descrito, (como é o caso das criações elencadas no artigo 10, conforme mencionamos).
A ABIFINA argumentou que há muitos anos a busca de novas formas
polimórficas para obter comportamento diverso de solubilidade, processabilidade, estabilidade de produtos químicos em fase sólida é prática rotineira nos laboratórios farmacêuticos e, portanto, é procedimento óbvio para técnicos no assunto:
Pequenas variações nas variáveis de processo podem causar o surgimento de novas formas polimórficas. Em operação a nível industrial, caracterizada por grandes volumes, é difícil conseguir absoluta homogeneidade de condições na massa reacional e não é raro constatar-se a presença de uma forma polimórfica predominante, mas com presença de outra forma em pequenas quantidades. Também no processamento de um fármaco para a preparação de um medicamento podem surgir condições que propiciem a passagem de uma forma polimórfica para outra. Para a caracterização da novidade e da atividade inventiva de um pedido de privilégio para o processo torna-se imprescindível que o mesmo seja descrito com precisão relacionando-se todos os parâmetros que caracterizam o processo como novo.
A decisão exarada pela 2a Turma Especializada do Tribunal Regional
Federal da 2ª Região, ilustra a questão, muito embora confundir descoberta com inventividade:
Das matérias referentes à propriedade industrial a patente de medicamentos e das mais controversas, por permitir uma serie de estratégias muito mais conceituais, do que inovadoras. Ou seja, a criatividade, no caso, fica por conta do desenvolvimento de estratégias conhecidas como life cycle management ou overgreening, que consistem no prolongamento de tempo do privilegio mediante a obtencao de múltiplas patentes, com base em diferentes atributos de um mesmo produto, visando a impedir, p. ex. a entrada de genéricos no mercado. A questão do polimorfismo se insere neste quadro. Desde os anos 60 que se sabe que substancias orgânica podem se apresentar, no estado solido, em diferentes formas, amorfas ou cristalinas, e que estas formas diferentes podem apresentar variações em algumas propriedades físicas como solubilidade, compressibilidade etc, propriedades estas que podem ser importantes para formulações farmacêuticas.
Patentes de polimorfos. Disponivel em:
Acesso em: 10/10/2012.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 136
Desde o final dos anos 80, problemas havidos com algumas formulações evidenciaram que o exato conhecimento do polimorfo usado na preparação de um medicamento era importante para a sua prescrição terapêutica correta. A partir de então, o estudo do polimorfismo das moléculas biologicamente ativas passou a ser rotina. E rotina e a antítese da inovação. Dai que a mera descoberta de formas polimórficas de um mesmo produto perdeu o atributo da inventividade, essencial para obtenção de uma patente. (grifo nosso). O "evergreening" não se esgota em polimorfos. Muitos outros tipos de patentes triviais, como sais diferentes da mesma molecula-base, segundo uso de princípios ativos já conhecidos, novas formulações de medicamentos em uso etc, são subterfúgios usados para obter novas patentes sobre velhas moléculas e assim, mediante táticas de modificação de registros, conseguir a manutenção da exclusividade de mercado e dos preços de monopólio de medicamentos. (AC 200551015078, 2a Turma Especializada do Tribunal Regional. Federal da 2a Região, por maioria. Rio de Janeiro, 22 de setembro de 2009. DES. FED. MESSOD AZULAY NETO).
Crucial também é atentar para as recomendações para o exame de
patentes farmacêuticas – WHO – ICTSD- UNCTAD
"Recomendación: El polimorfismo es una propiedad inherente a la materia en su estado sólido. Los polimorfos no se crean, sino que se descubren. Las oficinas de patentes deben tomar conciencia de la posible ampliación injustificada del período de protección, que surge del patentamiento sucesivo del principio activo y sus polimorfos, incluyendo hidratos/solvatos. Los procedimientos para obtener polimorfos pueden ser patentables en algunos casos, si demuestran ser novedosos y cumplen con el requisito de altura inventiva."
De igual importância é o Boletin Oficial de La Republica Argentina
Resolución Conjunta 118/2012, 546/2012 y 107/2012 Min. de Industria – Min. De Salud – INPI/AR "es uma propiedad inherente del estado sólido. Es decir, no es uma invención realizada por el hombre sino uma propriedad de la sustancia."
Correa alerta que as formas polimórficas na maioria das vezes não
contem um plus no estado de arte e, consequentemente, não são patenteáveis:
Solvates, including hydrates, were originally considered as "pseudo-polymorphs". Nevertheless, according to the International Conference of Harmonization (ICH) of 1999, they are to be deemed ‘polymorphs'. Hydrates/solvates will rarely be inventive, as they are obvious to produce in most situations. Hence, claims relating to changes in the content of water in known molecules (deriving in mono-hydrates, bi-hydrates, etc.) should generally be considered non-inventive and not patentable.
58 CORREA, Carlos. Guidelines for the examination of pharmaceutical patents, 2004.
59 CORREA, op. cit, p.11.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 137
Como já salientado, o polimorfismo se apresenta como uma propriedade
inerente da própria substância em estado sólido e em fases cristalinas, assim, é imprescindível cautela nos exames dos requisitos objetivos e técnicos utilizados em todos os casos para averiguar se há criação potencialmente inventiva capaz de abarcar temporariamente, a exclusividade patentária.
Neste contexto, a proposta formulada pelo INPI pode ser contestada
pelas seguintes razões:
(i) A atividade inventiva deve estar em consonância ao sistema
constitucional (a lei assegurará o interesse social e o desenvolvimento tecnológico e econômico do País.) ;
(ii) A abordagem problema/solução abrange passos sucessivos pré-
determinados e objetivos
(iii) Esta abordagem é apenas uma entre as possíveis para a aferição da
presença da atividade inventiv;
(iv) O silêncio quanto ao escopo dos limites de proteção de novas formas
polimórficas, o que a torna indubitavelmente preocupante devido as possíveis demandas judiciais por infração aos direitos patentários;
(v) A ausência de descrição minuciosa e precisa de todas as etapas e
divulgação de todos os parâmetros do processo pelo qual o "novo polimorfo" foi obtido.
Diz o artigo 13 que "a invenção é dotada de atividade inventiva sempre
que, para um técnico no assunto, não decorra de maneira evidente ou óbvia do estado da técnica".
O estabelecido no artigo 13 da lei 9.279/96 deve ser interpretado em
conformidade como texto constitucional que assegura a propriedade condicionada ao interesse social e ao desenvolvimento tecnológico e econômico do País.
Dessa maneira, o artigo traça parâmetros inquestionáveis quanto ao
exame para a aferição da presença deste contributo mínimo: a invenção (a) para um técnico no assunto, (b) ao tempo do depósito do pedido ou da prioridade, (c) não deve decorrer de maneira óbvia do estado da técnica.
60 Art. 5°, XXIX - a lei assegurará aos autores de inventos industriais privilégio temporário para sua utilização, bem como proteção às criações industriais, à propriedade das marcas, aos nomes de empresas e a outros signos distintivos, tendo em vista o interesse social e o desenvolvimento tecnológico e econômico do País.
61 SOUTO MAIOR, Rodrigo de Azevedo. As possibilidades da atividade inventiva no Brasil: uma busca no direito comparado pelos modos de aferição objetiva do critério de patenteabilidade, apresentada ao Programa de Mestrado em Direito Internacional da Faculdade de Direito da Universidade do Estado do Rio de Janeiro, 2009.
62 SOUTO MAIOR, Rodrigo Azevedo, op. cit.
63 Art. 13. A invenção é dotada de atividade inventiva sempre que, para um técnico no assunto, não decorra de maneira evidente ou óbvia do estado da técnica.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 138
Com efeito, deve as diretrizes de exame conter os procedimentos
necessários para que cada um destes parâmetros seja sistemático, claro e sindicável ao exame da atividade inventiva impedindo o desrespeito a cláusula constitucional ao se conceder patentes para invenções que não agregam de fato um state of art.
Assim, sempre que não estejam evidentemente conformes os requisitos
gerais de patenteamento segundo critérios estritos de exame, cabe efetivamente estabelecer um sistema de desincentivo a concessão de tais patentes através de exame mais rigoroso, compatíveis com o direito internacional aplicável ao país, como demonstra Barbosa
(a) A exigência de buscas feitas pelo examinador, de forma que o exame
não se resuma a simples repetição daqueles já executados no exterior, garantindo que em tais casos se efetuará o exame completo, e não o abreviado ou resumido;
(b) Que haja a comparação da busca independente e os achados em
buscas de outros escritórios de patentes;
(c) No caso de exame da atividade inventiva, que se explicite o método
seguido para determinação, garantindo assim o devido processo legal no caso de contestação desse aspecto técnico;
(d) A existência de um reexame necessário, por grupo de examinadores,
assegurando prazo máximo para essa providência, importando em denegação da pretensão se superado o termo regular de sessenta dias.
Além disso, o autor propõe a alteração da Lei 9.279/96 relativo às
patentes de segundo uso médico, seleção, segundo uso em geral (não só médico), reivindicações de simples formulação e às formas polimórficas, os isômeros, o tamanho das partículas, bem como a associação da substância com sais, ésteres, éteres e metabólitos: Texto a alterar, a saber:
Art. 29-A - Na apuração dos requisitos relativos aos art. 11 e 13,
realizados de acordo com o art. 229-C e o Capítulo III do Título I desta Lei, observando, no que couber, o disposto na Lei nº 9.784, de 29 de janeiro de 1999, será seguido regime específico no exame de invento relativo:
I – À modificação de produto terapêutico ou agroquímico compreendido
no estado da técnica, para a qual foi constatada emprego diverso daqueles já conhecidos;
II – Ao aspecto particular de um único elemento ou de um segmento
selecionado em um grupo maior, já constante do estado da técnica.
64 BARBOSA, Denis Borges. Polifôrmos, Enantiômetros & Coetera. Uma proposta de mudança legislativa, 2011, p. 53.
65 BARBOSA, op. cit., p. 51-52.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 139
III - A novas aplicações de produtos ou processos incluídos no estado da
técnica, ainda que o propósito para o qual devam ser usados difira daquele descrito no estado da técnica.
IV- A simples formulação, compreendendo produtos ou combinações já
constantes, individual ou coletivamente, do estado da técnica, ainda que se alegue efeito técnico novo.
V - Às formas polimórficas, os isômeros, o tamanho das partículas, bem
como a associação da substância com sais, ésteres, éteres, metabólitos, e ainda os complexos, combinações ou outros derivados do produto compreendido no estado da técnica. § 1º. Nas hipóteses deste artigo, o processo administrativo conterá:
I - transcrição completa, nos autos do processo administrativo, do
testemunho das buscas autônomas de anterioridades efetuadas diretamente pelo examinador, citando fontes e estratégia de busca, e justificando detalhadamente a eventual inexistência de novos achados;
II – o resultado das buscas realizadas por repartições de patentes
estrangeiras, em relação aos documentos a que a autarquia tenha convênio especial de acesso, se houver;
III – análise comparativa entre as fontes mencionadas nos incisos I e II
deste parágrafo.
IV – metodologia usada para análise referente ao art. 13 se tiver sido
demonstrada a satisfação do requisito do art. 11.
V – As razões pelas quais o examinador entenda haver suficiência
descritiva, que permita o pleno uso do objeto pretendido por terceiros, nas hipóteses legais em que caiba tal uso.
VI – A satisfação do requisito de aplicabilidade industrial, assim não se
considerando as hipóteses em que a tecnologia só possa ser implementada em caráter privado e pessoal, ou de outra maneira cuja reprodução implique em intervenção humana a cada caso. § 2º. Nas hipóteses dos incisos do caput deste artigo, o exame administrativo ou judicial não presumirá a existência dos requisitos dos art. 11 e 13 desta lei, incumbindo ao requerente ou titular prová-la. § 3º. Caso conclua pela existência dos requisitos dos art. 11 e 13, o examinador referirá automaticamente suas conclusões a grupo de revisão, constituído de três técnicos de igual ou superior qualificação, salvo se o pedido mereça indeferimento por aplicação de outros requisitos legais. § 4º. Ao fim de sessenta dias, salvo se a maioria dos revisores concluir pela existência dos pressupostos de patenteamento, dar-se-á por exarada a manifestação pelo indeferimento. § 5º. – Será assegurado ao titular do pedido e a todos interessados, nos termos desta Lei e, no que couber da Lei nº 9.784, de 29 de janeiro de 1999, o pleno acesso aos recursos e meios de defesa de seus interesses.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 140
Art. 13. A invenção é dotada de atividade inventiva sempre que, para um
técnico no assunto, não decorra de maneira evidente ou óbvia do estado da técnica.
Parágrafo único – Nas hipóteses do art. 29-A, a atividade inventiva será
reconhecida quando se apurar um progresso técnico relevante em face do
estado da técnica.
7. Considerações Finais
É necessário salientar que a concessão de patentes amplas, difusas e
mal examinadas seja de que área for, afetam negativamente o mercado e a sociedade em geral que acabam pagando um custo monopolístico indevido. O que caracteriza a patente como uso social da propriedade é o fato de que ela consiste em um direito limitado por sua função – existe quando socialmente útil. Tudo que representar o contrário é um contra direito.
"A lei de patentes não é um estatuto de proteção ao investimento – e
nem dos inventores; não é um mecanismo de internacionalização do nosso direito nem um lábaro nacionalista; é e deve ser lida como um instrumento de medida e ponderação, uma proposta de um justo meio e assim interpretado. E no que desmesurar deste equilíbrio tenso e cuidadoso, está inconstitucional".
Portanto, é imprescindível e indeclinável um exame cuidadoso e
concreto, respeitando caso a caso antes de se averiguar se um novo polimorfo de uma substância conhecida ou um processo de sua obtenção carecem de atividade inventiva. Assim, tanto o produto quanto o processo (art. 42, I e II) poderão ser patenteáveis (exceto ás criações em que a lei optou por não proteger por patentes) desde que resolvam um problema técnico diverso do anteriormente descrito e, principalmente, que satisfaçam todos os critérios objetivos exigidos pela lei 9.279/96.
Por fim, é necessário mencionar um problema que exige atenção: a lei
de propriedade intelectual ao regular o conteúdo jurídico das patentes de invenção diz no enunciado do artigo 42, I e II que a patente confere ao seu titular o direito de impedir terceiros, sem o seu consentimento, de produzir, usar, colocar à venda, vender ou importar com estes propósitos "processo" ou "produto" diretamente obtido por meio do processo patenteado. O que significa?
Significa que a concessão de patentes sobre um processo para a
criação de novas formas polimórficas conferirá ao titular os mesmo direitos de propriedade sobre o produto criado a partir do processo patenteado.
Portanto, é preciso cautela porque a proteção conferida aos produtos
fabricados com processos patenteados, a estes, se dará a tutela equivalente aos dos produtos advindos efetivamente do processo reivindicado.
66 BARBOSA, Denis Borges. Uma introdução à propriedade intelectual. Rio de Janeiro: Lumen Juris, 2003, p. 499.
67 BARBOSA, op. cit.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 141
Assim, como a matéria debatida se encontra em estado embrionário em
apreciação nos principais centros de patentes, não é viável e nem prudente para os órgãos administrativos competentes estabelecerem critérios de adequação antes de ser consolidada uma política sólida e sindicável de propriedade intelectual, com vistas, sempre ao interesse socioeconômico e tecnológico do País.
Será um contra senso e contrário ao interesse público quando não há no
momento, doutrinas sindicáveis e legislações eficazes para dirimir as celeumas
e alcançar um equilíbrio razoável quanto à proteção para estas espécies de
criações.
8. Referências
BARBOSA, Denis Borges. Tratado de propriedade intelectual. 5] § 2.1. Um
exemplo: a novidade no caso de cultivares. Rio de Janeiro: Lumen Juris, 2010,
p. 312.
. Tratado de propriedade intelectual. Seção 5, § 4 – a metodologia
para determinar a atividade inventiva. Rio e Janeiro: Lúmen Júris, 2010.
BARBOSA, Denis Borges et all. O contributo mínimo na propriedade intelectual:
Atividade Inventiva, Originalidade, distinguibilidade e margem mínima. Rio de
Janeiro: Lumen Juris, 2010, p. 10.
BARBOSA, Denis Borges, Research Handbook On The Protection Of
Intellectual Property Under WTO Rules, Intellectual Property in the WTO
Volume I, Edited by Carlos M. Correa, Director, Center for Interdisciplinary
Studies of Industrial Property and Economics, University of Buenos Aires,
Argentina.
. Serviços de Consultoria – Projeto PNUD/BRA/06/036-BSB-
Programa das Nações Unidas para o desenvolvimento, 2010.
BARBOSA, Pedro Marcos Nunes. As patentes farmacêuticas e os direitos
humanos. Cadernos da Escola de Direito e Relações Internacionais, v.2,
Curitiba, 2009, p. 13.
BRASIL. Lei 9.279/96. Regula direitos e obrigações relativos à propriedade
intelectual.
BRASIL. Lei 10.196/01. Altera e acresce dispositivos à Lei no 9.279, de 14 de
maio de 1996, que regula direitos e obrigações relativos à propriedade
industrial, e dá outras providências.
CARVALHO, Nuno Pires de. The TRIPS Regime of Trademarks and Designs.
USA: Ed. Kluwer Law Internacional, 2006, p.28-33.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Charlene de Ávila Plaza 142
CERQUEIRA, João da Gama. Tratado de propriedade intelectual, v.II, tomo I, parte II, Rio de Janeiro: Revista Forense, 1952, p. 320. CORREA, C. M. Propriedade Intelectual e Saúde Publica. 1ª edição, La ley, Buenos Aires, 2006. _. Trade Related Aspects of Intellectual Property Rights, p.311-345. _. Guidelines for the examination of pharmaceutical patents, 2004. CHAVANNE e Burst. Droit de La propriété industrielle, Dalloz, 1990, n. 16 e seg., p. 33-34. LEONARDOS, Luiz; OSWALD, Maria Cecília. Direito de patentes: uma resposta de filtragem constitucional. Revista da ABPI, 2007, p. 10. LIMA, Denise M. Menezes de; SILVEIRA, Carla Cristina de Freitas. Physis Revista de Saúde Coletiva. Rio de Janeiro, 2011, p. 1520-21. LOVE, James. Remuneration Guidelines for non-voluntary use a patent on medical Technologies – WHO/TCM/2005, Geneva, 2005. MENDONÇA, José Xavier Carvalho de. Tratado de direito comercial brasileiro apud BARBOSA, Denis Barbosa. O Código de propriedade intelectual conforme os tribunais, 2011, p. 131, no prelo. MIRANDA, Pontes de. Tratado de Direito Privado. São Paulo: Revista dos Tribunais, v. 4, 1983, p. 274. MUSUNGU, Sisuli e OH, Cecília. The Use of Flexibilities in TRIPS BY Developing Countries. World Health Organization, 2006, p. 19. POLLAUD Dullian. La brevetabilité dês inventions, Litec, 1997, p.41 PLAZA, Charlene de Ávila. Notas sobre patentes e certificados de cultivares: conflitos ou complementos de proteção? Revista da ABPI, n. 118, mai/jun de 2012, p. 12. PLAZA, Charlene de Ávila. Recentes precedentes da Comunidade Europeia em propriedade intelectual. Revista da ABPI, 116, 2012. RAIMUNDO Jorge. Patentes polimórficas e patentes de segundo uso médico, 2009. SOUTO MAIOR, Rodrigo de Azevedo. As possibilidades da atividade inventiva no Brasil: uma busca no direito comparado pelos modos de aferição objetiva do critério de patenteabilidade, apresentada ao Programa de Mestrado em Direito Internacional da Faculdade de Direito da Universidade do Estado do Rio de Janeiro, 2009.
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
NOTAS SOBRE PATENTES DE NOVAS FORMAS POLIMÓRFICAS ISSN ELETRÔNICO 2316-8080 143
Recebido no dia 19/10/2012
Aprovado no dia 22/10/2012 Publicado no dia 30/10/2012
PIDCC, Aracaju, Ano I, Edição nº 01/2012, p.106 a 143 Out/Dez 2012
Source: http://www.pidcc.com.br/artigos/102012/102012_04.pdf
Inhibitory Contributions to Spatiotemporal Receptive-Field Structureand Direction Selectivity in Simple Cells of Cat Area 17 ADITYA MURTHY AND ALLEN L. HUMPHREYDepartment of Neurobiology, University of Pittsburgh School of Medicine, Pittsburgh, Pennsylvania 15261 Murthy, Aditya and Allen L. Humphrey. Inhibitory contributions spond well to motion in one direction across their receptive
ISSN: 2454-2415 Volume 2, Issue 1, January, 2016 International Journal of Innovative Knowledge Concepts Premenstrual Symptoms and Social Disability Nabhit Kapur1 and Prabhjeet Singh Narula2 1Director ,Peacfulmind training center Asst Coordinator, Peacfulmind Training Center Abstract :










